Ảnh hưởng của thức ăn khác nhau đến tỷ lệ sống và tỷ lệ lột vỏ của cua xanh (Scyllasp.) nuôi trong bể tuần hoàn
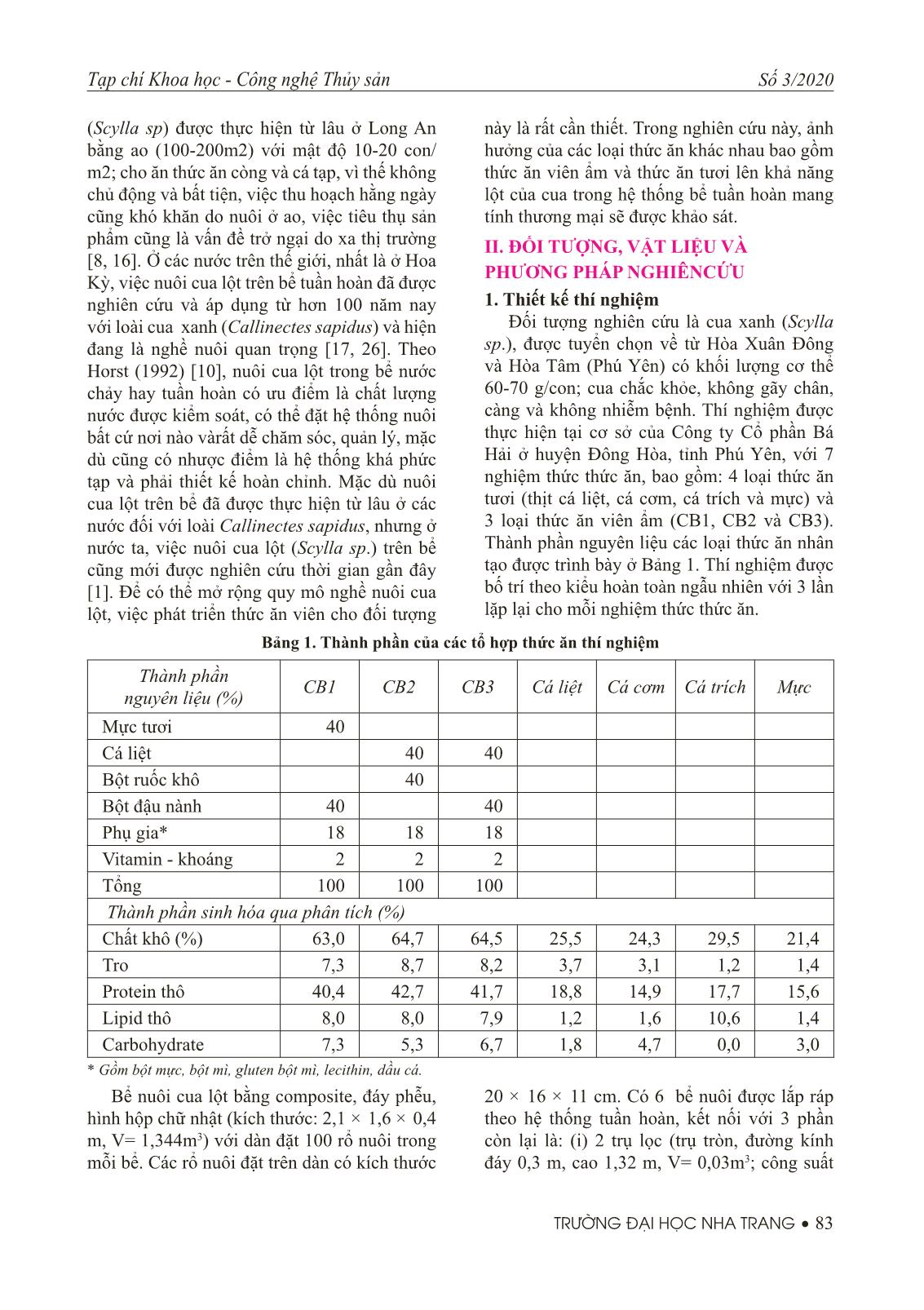
TÓM TẮT Nghiên cứ u nuôi cua xanh (Scylla sp) lộ t trong hệ thố ng tuầ n hoà n tại cơ sở của Công ty Cổ phần Bá Hải ở huyện Đông Hòa, tỉnh Phú Yên với 7 nghiệm thức thức ăn, bao gồm: 4 loại thức ăn tươi (thịt cá liệt, cá cơm, cá trích và mực) và 3 loại thức ăn viên ẩm (CB1, CB2 và CB3). Mỗi nghiệm thức được lặp lại 3 lần. Sau 5 tuần thí nghiệm, tỷ lệ sống của cua được cho ăn thức ăn CB2(40% cá liệ t + 40 % bộ t ruố c + 18% phụ gia + 2% Vitamin, khoá ng) là cao nhất (95%) và sai khác có ý nghĩa với cua được cho ăn các loại thức ăn còn lại (88-91%) (P<0,05); tỷ="" lệ="" lột="" vỏ="" của="" cua="" được="" cho="" ăn="" thịt="" cá="" cơm="" là="" thấp="" nhất="" (73%)="" và="" sai="" khác="" có="" ý="" nghĩa="" với="" cua="" được="" cho="" ăn="" các="" loại="" thức="" ăn="" còn="" lại="" (83,3-87,5%)=""><0,05). từ="" kết="" quả="" thí="" nghiệm="" có="" thể="" thấy="" rằng="" nuôi="" cua="" xanh="" lột="" trong="" bể="" tuần="" hoàn="" bằng="" thức="" ăn="" viên="" cb2="" cho="" tỷ="" lệ="" sống="" và="" tỷ="" lệ="" lột="" vỏ="" tốt="">

Trang 1
Trang 2

Trang 3

Trang 4

Trang 5

Trang 6

Trang 7
Tóm tắt nội dung tài liệu: Ảnh hưởng của thức ăn khác nhau đến tỷ lệ sống và tỷ lệ lột vỏ của cua xanh (Scyllasp.) nuôi trong bể tuần hoàn

trụ lọc (trụ trò n, đườ ng kí nh đá y 0,3 m, cao 1,32 m, V= 0,03m3; công suất 84 • TRƯỜNG ĐẠI HỌC NHA TRANG Tạp chí Khoa học - Công nghệ Thủy sản Số 3/2020 1,8 m3/giờ. Trụ 1: dùng cho lọc thô, sử dụng đá sỏi và cát làm vật liệu lọc với tỷ lệ cát, sỏi và đá là 1:0,5:0,5. Trụ 2: hấp thụ ammonia bằng vật liệu Clino X). (ii) Skimer (máy tách đạm). (iii) 2 bể chứa (kích thước: 1,7 x 1,4 x 0, 8 m, V=1,9 m3) được làm bằng composite. Tỉ lệ V nuôi: V xử lý = 2. Do tổng số cua được theo dõi cho mỗi nghiệm thức nghiên cứu là 150 con trong khi tổng số cua nghiên cứu mỗi đợt tối đa là 600 con, nên thí nghiệm chia làm hai đợt với số lượng cua theo dõi cho mỗi nghiệm thức ở mỗi đợt là 75 con. Số liệu thu được từ hai đợt sẽ được tổng hợp và phân tích.Việc quan sát được tiến hành hàng ngày, đặc biệt khi cua vào giai đoạn lột vỏ. Các chỉ số theo dõi bao gồm: tỷ lệ sống và tỷ lệ lột vỏ tự nhiên. Nhiệt độ nước được đo hàng ngày bằng nhiệt kế thủy ngân. Hàm lượng oxy hòa tan (DO) được xác định 3 ngày một lần cho mỗi bể thông qua sử dụng O2 Sera test kit. Ngoài ra, pH, độ mặn, alkalinity, NO2 - và hàm lượng total ammonia nitrogen (TAN) cũng được xác định cách khoảng 3 ngày. Độ mặn được xác định bằng khúc xạ kế cầm tay (France); pH, NO2 -, alkalinity và hàm lượng TAN được xác định qua các bộ Sera test kit pH, NO2 -, Alkalinity và NH4/NH3 (Germany), theo thứ tự tương ứng. 2. Các phương pháp phân tích 2.1. Phân tích hoá học Việc phân tích được tiến hành tại Trung tâm Thí nghiệm – Thực hành, Trường Đại học Nha Trang. Các mẫu nguyên liệu thức ăn, thức ăn được phân tích theo Hệ thống phân tích thô, gồm nhiều phương pháp nhỏ nhằm tách mẫu phân tích thành các nhóm dưỡng chất khác nhau như độ ẩm, protein, lipid, tro, xơ và chiết chất không chứa Ni-tơ. Protein thô được tính như sau: CP = N x 6,25. Hàm lượng Ni-tơ được xác định theo Phương pháp Kjeldahl. Hàm lượng lipid tổng số được phân tích bằng Phương pháp Folch. 2.2. Phân tích thống kê Số liệu được xử lý thống kê trên các phần mềm SPSS và Excel. Phép kiểm định Duncan’s Multiple Range được sử dụng để kiểm tra sự khác nhau giữa các trung bình nghiệm thức. Các sai khác được đánh giá có ý nghĩa ở mức P<0,05. III. KẾT QUẢ NGHIÊN CỨU VÀ THẢOLUẬN 1. Các yếu tố môi trường nước nuôi Nhìn chung, các yếu tố môi trường của thí nghiệm nằm trong phạm vi thích ứng của cua (Bảng 2). Cụ thể là: cua biển có phạm vi nhiệt độ thích ứng là 23 - 35ºC [18, 20], nhưng tối ưu là trong khoảng 25 - 30ºC [4, 20]; cua có thể chịu đựng độ mặn trong phạm vi 2-60‰ [9] và tối ưu trong khoảng 10 - 25‰ [20]. Phạm vi pH thích ứng cho tôm, cua biển là 6-9 [5], và tối ưu là 7,8- 8,2 [4; 25]. Hàm lượng oxy hòa tan thích hợp là DO > 3 mg/l. Hiện vẫn chưa có những nghiên cứu cụ thể về ngưỡng thích ứng về độ kiềm và ngưỡng chịu đựng Nitrite và NH3 đối với cua. Tuy nhiên, các nghiên cứu trên tôm he cho thấy: Phạm vi độ kiềm thích ứng (mg CaCO3/l) là 80- 200 mg/l [7]; Hàm lượng ammonia (NH3-mg/l) thích ứng là nhỏ hơn 0,3 mg/l [3, 13]; Hàm lượng nitrite (NO2 -- mg/l) thích ứng là nhỏ hơn 5 mg/l [14, 23]. Nhìn chung, diễn biến các yếu tố độ kiềm, Nitrite và Ammonia đều nằm trong phạm vi thích hợp cho tôm he cũng như các động vật biển khác. Bảng 2. Các yếu tố môi trường trong suốt thời gian thí nghiệm Yếu tố Sáng Chiều Nhiệt độ nước (oC) 26,8 ± 1,17 28,5 ± 1,05 Độ mặn (‰) 15,0 ± 0,63 pH 7,5 – 7,8 7,7 - 8,0 Oxy hòa tan (mg/L) 6,5 ± 0,43 6,5 ± 0,38 Độ kiềm (mg/L) 113,3 ± 5,16 Nitrite (mg/L) 0,3-0,5 Ammonia (NH3-mg/L) 0,09 – 0,14 Tạp chí Khoa học - Công nghệ Thủy sản Số 3/2020 TRƯỜNG ĐẠI HỌC NHA TRANG • 85 2. Tỷ lệ sống, tỷ lệ cua lột vỏ Kết quả từ Bảng 3 cho thấy: tỷ lệ sống của cua trong quá trình thí nghiệm là rất cao (≥88%), trong đó cao nhất là ở nghiệm thức thức ăn CB2 (95%). Tỷ lệ sống của cua ăn thức ăn CB2 khác biệt có ý nghĩa với các trường hợp còn lại (P<0,05). Tỷ lệ sống của cua được nuôi bằng các loại thức ăn còn lại không sai khác có ý nghĩa với nhau (P>0,05). Tỷ lệ của lột vỏ thấp nhất là ở nghiệm thức thức ăn cá cơm (73%) và tỷ lệ này khác biệt có ý nghĩa so với các trường hợp còn lại (P<0,05). Với các loại thức ăn còn lại, đã không có khác biệt có ý nghĩa về tỷ lệ cua lột vỏ (P>0,05). Như vậy, sơ bộ đánh giá chung có thể thấy thức ăn CB2 cho tỷ lệ sống và tỷ lệ cua lột vỏ cao nhất, còn thức ăn cá cơm thì ở phía ngược lại. Bảng 3. Tỷ lệ sống và tỷ lệ lột vỏ của cua thí nghiệm Thức ăn Tỷ lệ sống (%) Tỷ lệ cua lột vỏ (%) CB1 90,0 a 83,5 b CB2 95,0 b 84,5 b CB3 91,0 a 87,5 b Cá liệt 89,3 a 83,3 b Cá cơm 90,0 a 73,0 a Cá trích 89,0 a 83,5 b Mực 88,0 a 84,0 b ±SEM 0,62 4,85 a,b Cùng một cột, các giá trị trung bình có ký tự không giống nhau thể hiện khác biệt có ý nghĩa (P<0,05). Cua biển thuộc nhóm giáp xác ăn tạp thiên về động vật. Trong thực tế nuôi, cua biển hầu như không được cho ăn khi nuôi quảng canh trong đầm hay cho ăn bằng cá tạp, rạm, còng hay nhuyễn thể khi nuôi trong lồng và ao [1, 8, 12, 16, 19]. Tuy nhiên, nhiều nghiên cứu cho thấy các loài cua biển trong nhóm Scylla spp. vẫn có thể sử dụng thức ăn chế biến ở các mức độ khác nhau. How-Cheongvà cộng sự (1992) [11] lần đầu tiên công bố việc nghiên cứu thức ăn nhân tạo cho cua biển (Scylla serrata) và cho rằng có thể sử dụng thức ăn nhân tạo nuôi cua thịt cho kết quả tăng trưởng khá tốt với hàm lượng protein 35-40%. Nghiên cứu của Unnikrishnan (2006) [25] cho thấy: mức protein thô (CP) tối ưu trong thức ăn của của nên nằm trong khoảng 40-45%. Trong thức ăn tổng hợp dùng nuôi cua Scylla serrata, Sheen và Wu (1999) [21] đã khuyến cáo mức 5,3 đến 13,8% lipid dưới dạng một hỗn hợp của dầu gan cá tuyết và dầu bắp ở tỷ lệ 2:1. Catacutan (2002) [6] cũng cho rằng, cua tăng trưởng tốt với thức ăn nhân tạo chứa 32-40% protein ngay khi lipid 6% hay 12%. Smith và cộng sự (2014) [22] cũng cho rằng thức ăn cho cua Scylla serata nên có hàm lượng protein thô và năng lượng thô lần lượt là CP≥40% và GE≥18 MJ/ kg thức ăn. Các kết quả nghiên cứu của các tác giả này hầu hết trên đối tượng cua biển Scylla serrata, nhưng là nguồn tham khảo quan trọng cho cho việc nghiên cứu trên đối tượng cua biển S. paramamosain và S. olivacea ở nước ta. Để tiện so sánh, số liệu thành phần sinh hóa của tất cả các tổ hợp thức ăn được quy đổi về 90% chất khô (là mức tối thiểu của thức ăn viên khô) như được thể hiện trong Bảng 4. Qua bảng này có thể thấy: tất cả các tổ hợp thức ăn đều thỏa mãn các chỉ tiêu kỹ thuật của thức ăn dùng để nuôi cua (CP ≥ 40%, TL=5,3-13,8% và GE ≥18 MJ/kg) trừ thức ăn cá trích có hàm lượng lipid vượt quá mức nhu cầu (32,3%) và thức ăn cá liệt có hàm lượng lipid hơi thấp (4,1%). Ngoài ra, thức ăn cá cơm và cá trích có hàm lượng protein hơi thấp so với các tổ hợp thức ăn còn lại. Khác với tôm, cua chuộng thức ăn có hàm lượng lipid cao hơn [2] và dĩ nhiên trong phạm vi thích ứng của mình, do đó các tổ hợp thức ăn viên (CB1, CB2 và CB3) dường như phù hợp hơn về khía cạnh lipid so với các loại thức ăn tươi (cá liệt, cá cơm và 86 • TRƯỜNG ĐẠI HỌC NHA TRANG Tạp chí Khoa học - Công nghệ Thủy sản Số 3/2020 mực). Rõ ràng thức ăn cá cơm có hàm lượng protein, lipid cũng như năng lượng thô đều thấp so với các tổ hợp thức ăn khác, trong khi đó thức ăn CB2 lại có các chỉ số tương ứng cao và cân bằng hơn giữa protein và lipid. Ngoài ra, thức ăn CB2 còn chứa thành phần thức ăn giáp xác (Bảng 1) mà các tổ hợp thức ăn khác không có. Đây cũng có thể là yếu tố thúc đẩy sự lột xác của cua. Để đảm bảo quá trình lột vỏ tốt, cua đã phải huy động một lượng vật chất (protein) và năng lượng (chủ yếu từ lipid) rất lớn, do vậy chỉ những loại thức ăn vừa đảm bảo nhu cầu dinh dưỡng thông thường vừa đảm bảo tăng cường vật chất và năng lượng cho lột vỏ mới đáp ứng được yêu cầu duy trì (thể hiện qua tỷ lệ sống) và phát triển (thể hiện qua tỷ lệ lột vỏ) của cua. Lập luận này cũng được khẳng định phần nào từ kết quả phân tích thành phần dinh dưỡng của cua chắc và cua lột, theo đó cua chắc có hàm lượng protein cao hơn cua lột nhưng cua lột có hàm lượng lipid và khoáng cao hơn cua chắc [1]. Bảng 4. Thành phần sinh hóa của các tổ hợp thức ăn thí nghiệm qua quy đổi CT1 CT2 CT3 Cá Liệt Cá Cơm Cá Trích Mực Chất khô (%) 90,0 90,0 90,0 90,0 90,0 90,0 90,0 Tro 10,4 12,1 11,5 13,1 11,6 3,7 5,9 Protein thô 57,7 59,5 58,1 66,4 55,0 54,0 65,6 Lipid thô 11,5 11,1 11,0 4,1 6,0 32,3 5,9 Carbohydrate 10,4 7,4 9,4 6,5 17,4 0,0 12,6 GE (kJ/g) 19,8 19,5 19,5 18,2 18,2 25,3 19,8 Ngoài ra, nghiên cứu này cũng cho thấy, việc nuôi cua lột trên bể tuần hoàn quy mô sản xuất (>1000 L/bể) vớ i tỉ lệ Vnuôi / Vxử lý = 2 nhìn chung rất tiện lợi trong quản lý và chăm sóc. Đây là yếu tố quan trọng để có thể tiếp tục nghiên cứu ứng dụng mô hình này so với việc nuôi trong ao hoặc bể tuần hoàn với quy mô phòng thí nghiệm (~100 L/bể) như đã được triển khai trước đây [1]. IV. KẾT LUẬN VÀ KIẾN NGHỊ 1. Kết luận • Hệ thống tuần hoàn (>1000 L/bể nuôi), vớ i tỉ lệ Vnuôi / Vxử lý = 2 đã bả o đả m cá c yế u tố môi trườ ng nuôi thí ch hợ p và ổ n đị nh trong suố t quá trì nh thí nghiệ m. • Tỷ lệ sống của cua trong quá trình thí nghiệm là rất cao (≥88%) và cao nhất là ở nghiệm thức thức ăn CB2 (95%). Tỷ lệ sống của cua ăn thức ăn CB2 khác biệt có ý nghĩa với các trường hợp còn lại (P<0,05). Tỷ lệ sống của cua được nuôi bằng các loại thức ăn còn lại không sai khác có ý nghĩa (P>0,05). • Tỷ lệ cua lột vỏ thấp nhất ở nghiệm thức thức ăn cá cơm (73%) và tỷ lệ này khác biệt có ý nghĩa so với các trường hợp còn lại (P<0,05). Tỷ lệ lột vỏ của cua được nuôi bằng các loại thức ăn còn lại không sai khác có ý nghĩa (P>0,05). 2. Kiến nghị • Nghiên cứu hoàn thiện thức ăn công nghiệp nuôi cua lột quy mô sản xuất lớn. LỜI CẢM ƠN Tác giả cảm ơn Ban lãnh đạo Công ty Cổ phần Bá Hải đã tạo điều kiện để tiến hành thí nghiệm này tại cơ sở của công ty. TÀI LIỆU THAM KHẢO Tiếng Việt 1. Trần Ngọc Hải, Nguyễn Thanh Phương, Nguyễn Anh Tuấn và Phạm Minh Đức, 2006. Nuôi cua lột Scylla sp. trong hệ thống tuần hoàn với các loại thức ăn và mật độ khác nhau. Tạp chí Nghiên cứu Khoa học Trường Đại học Cần Thơ, Số 2006: 159-170. Tạp chí Khoa học - Công nghệ Thủy sản Số 3/2020 TRƯỜNG ĐẠI HỌC NHA TRANG • 87 Tiếng Anh 2. Anderson, A., Mather P., and Richardson N., 2004. Nutrition of the mud crab, Scylla serrata (Forskal). In: Allan G. and Fielder D. (Eds), Mud crab aquaculture in Australia and Southeast Asia. ACIAR working paper No. 54. 57-60.Asian fi sheries science, special issue,14, 231-238. 3. Alves, C.S., Mello, G.L., 2007. Manual para o Monitoramento Hidrobiológico emFazendas de Cultivo de Camarão. Recife, Pernambuco. 4. Baliao, D.D., D.S. Santos, M.A., and Franco, N.M., 1999. Mudcrab, Scylla spp, production in Brackishwater Ponds. Aquaculture Department Southeast Asian Fisheries, Development Center, Tigbauan, Iloilo, Philippines. 5. Boyd, C.E., 1990. Water quality in warmwater fi sh ponds. Agricultural Experimentation. Auburn University, Opelika, Alabama, USA. 359p. 6. Catacutan, M. R. 2002. Growth and body composition of juvenile mud crab, Scylla serrata, fed different dietary protein and lipid levels and protein to energy ratios. Aquaculture, 208,113-123. 7. Ching, C.A. 2007. Water alkalinity in the cultivation of marine shrimp. Bouletines Nicovita 3:1-3. 8. Dat, H.D., 1999. Description ofmud crab (Scylla spp.) culture methods in Vietnam. In Keenan (Ed): Mud Crab Aquaculture and biology. ACIAR proceedings No 78,67-71. 9. Hill, B.J., 1974. Salinity and temperature tolerance of Zoea of Portunid crab (Scylla serrata). Marine Biology, 32, 119-126. 10. Horst J. (1992). Soft-shelled crab roduction – Obtions and opportunities. Louisiana Sea Grat College Programe. 13 pp. 11. How-Cheong, C., Gunasekera U.P.D and Amandakoon, 1992. Formulation of Artifi cial feeds for mud crab culture: A preliminary biochemical, physical and biological evaluation. In C.A. Angell (ed): The Mudcrab. Report of the seminar on the mud crab culture and trade, Bay of Bengal Programme, pp. 179-184. 12. Johnston, D. and Keenan C.P., 1999. Mud crab culture in Minh Hai province, South Vietnam. In Keenan (Ed): Mud Crab Aquaculture and biology. ACIAR proceedings No 78,95-98. 13. Lin, Y.C., and Chen, J.C. 2001. Acute toxicity of ammonia on Litopenaeus vannamei Boone juveniles at different salinity levels. Journal of Experimental Marine Biology and Ecology 259:109-119. 14. Lin, Y.C., and Chen, J.C. 2003. Acute toxicity of nitrite on Litopenaeus vannamei (Boone) juveniles at different salinity levels. Aquaculture 224:193-201. 15. Macintosh, D.J.; Overton, J.L.; Thu, H.V.T., 2002. Confi rmation of two common mud crab species (Genus Scylla) in the mangrove ecosystem of the Mekong Delta, Vietnam. Journal of Shelfi sh Research; 21(1),259-265 16. Nguyen Anh Tuan và Tran Ngoc Hai, 1997. Culture mud crab Scylla serrata in the Mekong Delta, Vietnam. Paper presented at the First International Conference, Kuala Terrenganu, Malaysia. 17. Oesterling, M. J., 2002. Soft crab in closed systems: A Virginia success story. In: Proceedings of the 1st International Conference on Recirculating Aquaculture. 18. Ong, K.S., 1966. Observation on the Post-Larval Life History of Scylla serrata Forskal Reared in the Laboratory. The Malavsian Agricultural Journal, 45,429-443. 19. Say, W.C. W. and Ikhwanuddin, A. Mhd., 1999. Pen culture of mud crabs, Genus Scylla in the mangrove Ecosystems of Sarawak, East Malaysia. In Keenan (Ed): Mud Crab Aquaculture and biology. ACIAR proceed- ings No 78,83-88. 20. Shelley, C., Lovatelli, A.,2011. Mud crab aquaculture - A practical manual, FAO Fisheries and Aquaculture Technical Paper. No. 567. Rome, FAO. 2011. 78 pp. 88 • TRƯỜNG ĐẠI HỌC NHA TRANG Tạp chí Khoa học - Công nghệ Thủy sản Số 3/2020 21. Sheen, S. S. and S. W. Wu. 2003. Essential fatty acid requirements of juvenile mud crab, Scylla serrata (Forskal, 1775) (Decapoda, Scyllaridae). Crustacean a, 75 (11): 1387-1401 22. Smith D. and Tuan, L.A., 2014. Nutritional requirements of tropical crustaceans. Paper presented at the training workshop held at Nha Trang University, March 19th -21st, 2014. 23. Timmons, M.B., and Ebeling, J.M. 2007. Recirculating Aquaculture. Cayuga Aqua Ventures, Ithaca, New York. 24. Trino, A. T.; Rodriguez, E. M., 2002. Pen culture of mud crab Scylla serrata in tidal fl ats reforested with mangrove trees. Aquaculture, 211, 125-134. 25. Unnikrishnan U., 2006. Nutritional value of fresh processed and formulated diets for the green mud crab Scylla serrata juveniles. PhD Thesis, Cochin University of Science & Technology, India. 26. Webster, D., 1998. Soft crabs and recirculating systems. Aquaculture magazine, 24, 23-24.
File đính kèm:
 anh_huong_cua_thuc_an_khac_nhau_den_ty_le_song_va_ty_le_lot.pdf
anh_huong_cua_thuc_an_khac_nhau_den_ty_le_song_va_ty_le_lot.pdf

