Ứng dụng chiết điểm mù sử dụng 1-(2-pyridylazo)-2-naphthol và Triton X-100 phân tích dạng mangan trong mẫu chè
A simple, rapid, inexpensive, and nonpolluting cloud point extraction (CPE) technique has been
improved for the preconcentration and determination of species manganese in tea infusion. The
optimization step was performed involving the following variables: pH, concentration of 1-(2-
pyridylazo)-2-naphtol (PAN) and Triton X-100 (TX-100), incubation temperature, incubation time and
ionic strength (with concentration NaCl). Under the optimized conditions, enrichment factor of 8,3 was
achieved leading to limit of detection and limit of quantitation of 0.0308 and 0.0935 ppm, respectively.
In tea infusion, flavonoid bound Mn(II) and weakly complexed Mn(II) occupy for 6,05 – 15,3%, 84,7 –
93,95% respectively.

Trang 1

Trang 2

Trang 3
Trang 4
Trang 5
Trang 6
Trang 7

Trang 8
Tóm tắt nội dung tài liệu: Ứng dụng chiết điểm mù sử dụng 1-(2-pyridylazo)-2-naphthol và Triton X-100 phân tích dạng mangan trong mẫu chè

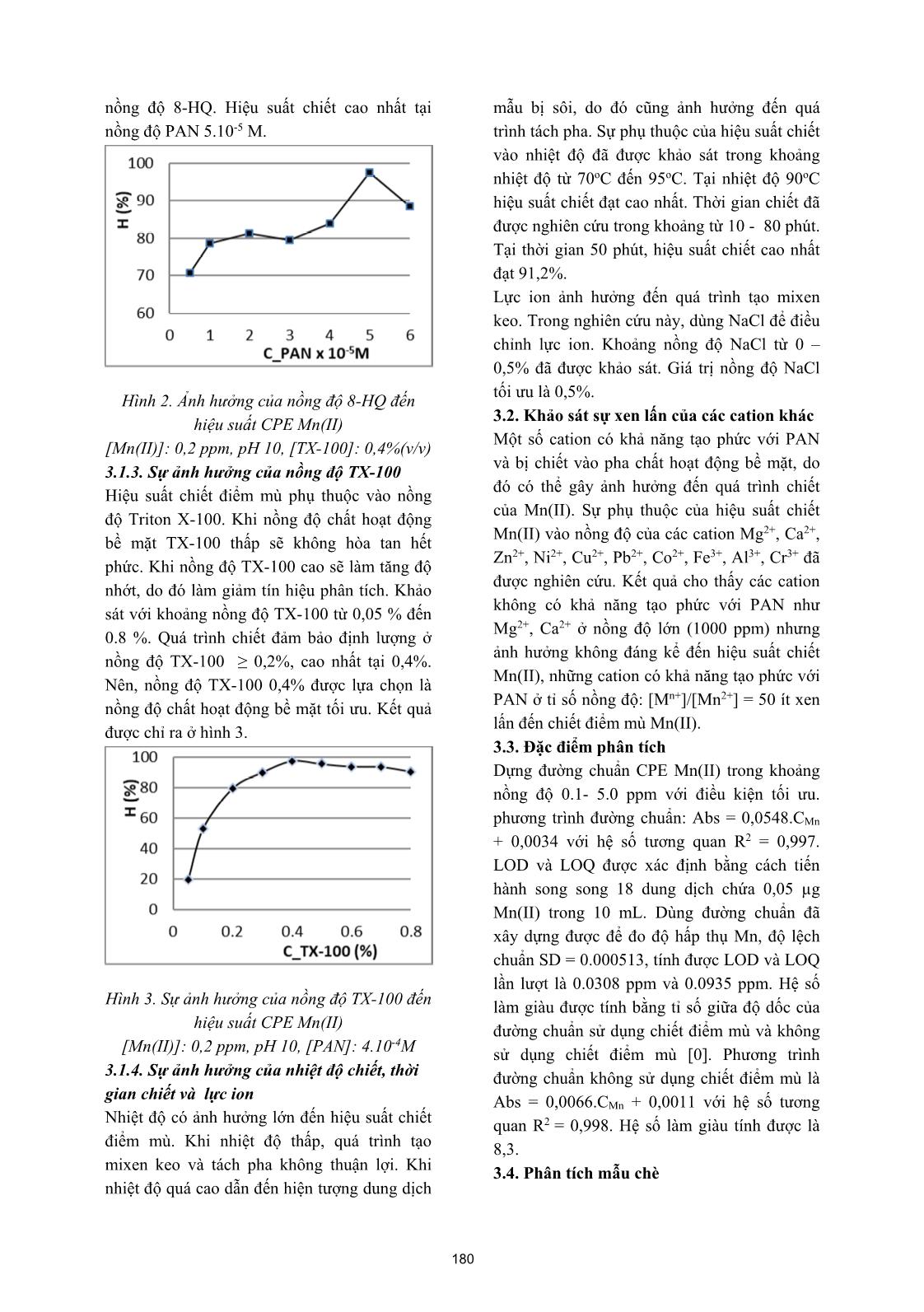
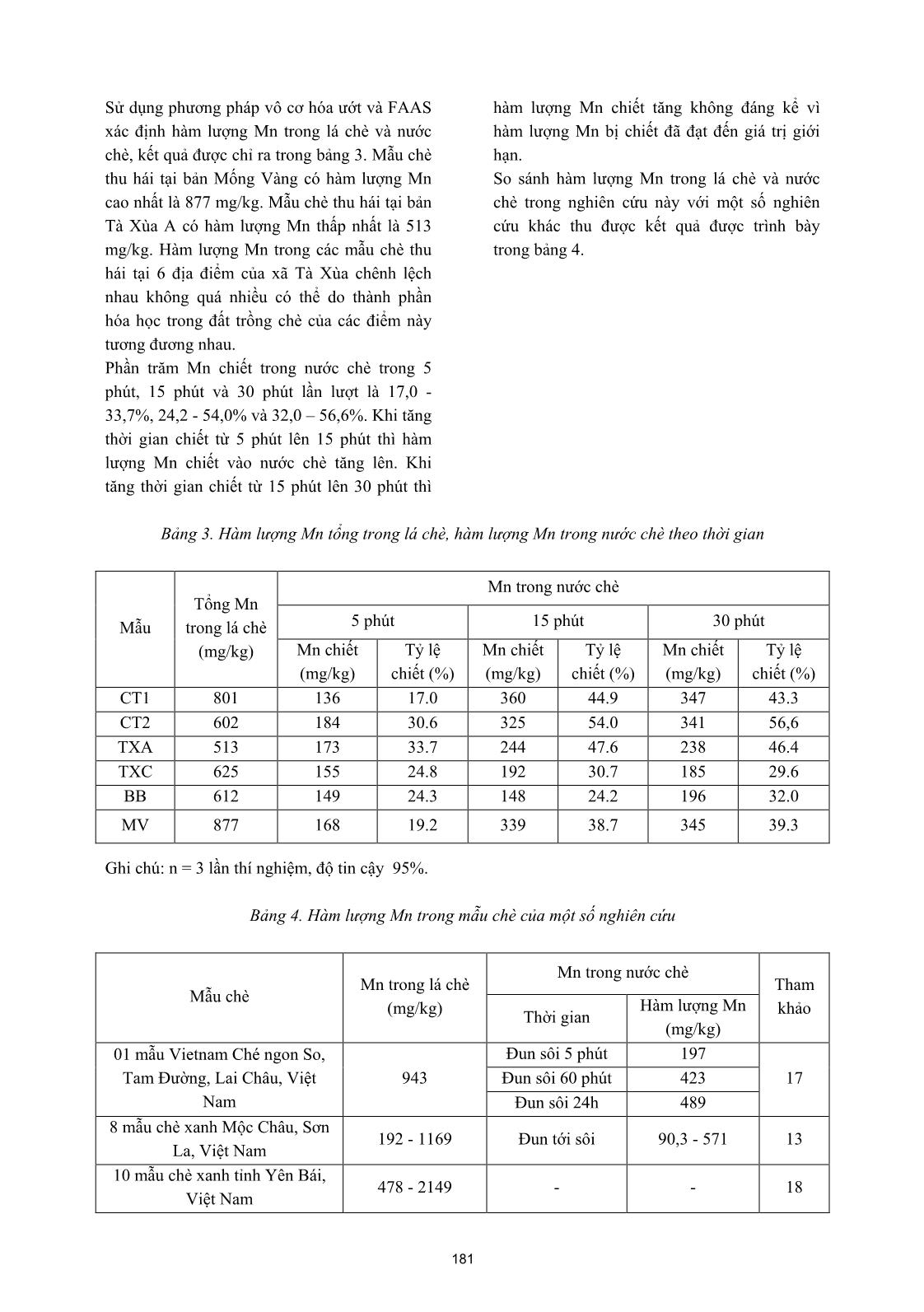
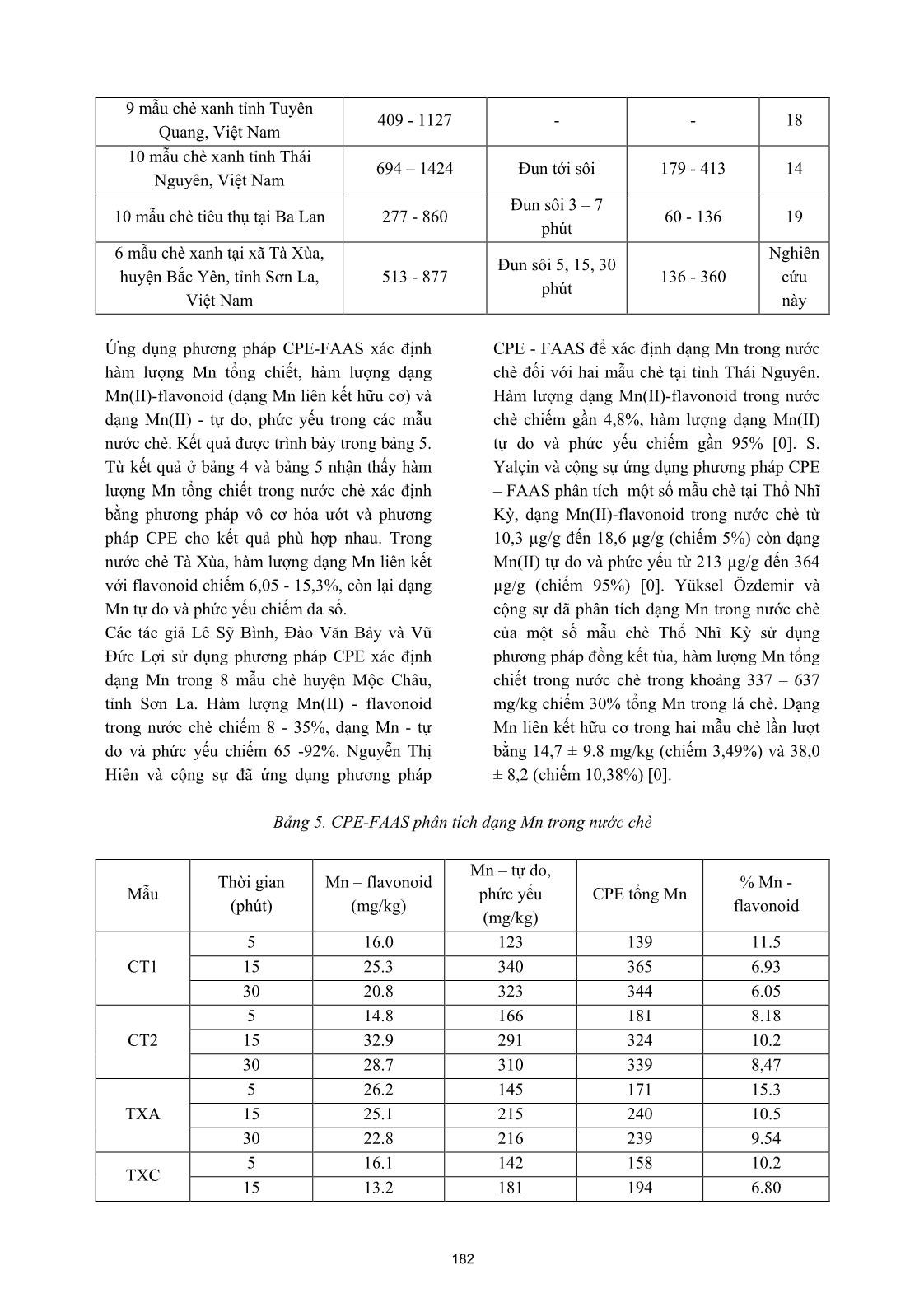
iá trị pH: 6 (đệm axetat), 7 nhất mẫu bằng máy lắc. Phân tích hàm lượng (đệm photphat - borat), 8, 9, 10, 11 (đệm borat) Mn tổng trong nước chè bằng FAAS. Mẫu [0]. Kết quả được chỉ ra ở Hình 1, ở giá trị pH trắng được tiến hành tương tự thay 1,0 mL 10 hiệu suất chiết Mn (H%) cao nhất đạt 87,6 nước chè bằng 1,0 mL nước cất. (%). Do đó, dung dịch đệm pH 10 borat được 2.6.2. Xác định dạng Mn (II)- flavonoid trong lựa chọn để tiến hành các thí nghiệm tiếp theo. nước chè Khảo sát với thể tích dung dịch pH 10 borat Lấy 2,0 mL nước chè, thêm 1,0 mL TX-100 trong khoảng 0.25 – 3.0 mL. Kết quả thu được, 4% (v/v), 1,0 mL dung dịch NaCl 5%, cuối thể tích dung dịch đệm tối ưu là 2,0 ml. cùng dung dịch được pha loãng tới 10 mL bằng nước cất. Các bước tiếp theo tiến hành giống như 2.6.1. 2.6.3. Xác định dạng Mn(II) - tự do và phức yếu trong nước chè Sau khi CPE tách dạng Mn(II)-flavonoid trong nước chè, dạng Mn(II) tự do và phức yếu (phức với các ion vô cơ) vẫn còn tồn tại trong pha nước sẽ được tạo phức với PAN và chiết, làm giàu bằng TX-100. Quy trình như sau: 5,0 Hình 1. Ảnh hưởng của pH đến hiệu suất chiết mL pha nước ở trên, thêm 1,0 mL dung dịch [Mn(II)]: 0,2 ppm, [PAN]: 5.10-5M, [TX-100]: -3 PAN 2.10 M và 1,0 mL TX-100 4%, thêm 2,0 0,4% mL đệm pH 10 (borat), thêm 1,0 mL dung dịch 3.1.2. Sự ảnh hưởng của nồng độ PAN NaCl 5%, định mức đến 10 mL bằng nước cất. Khảo sát tìm nồng độ tối ưu của PAN khi cố Các bước tiếp theo tiến hành giống như 2.6.1. định các yếu tố khác như: pH, nồng độ TX-100, 2.7. Khảo sát tìm điều kiện tối ưu đối với thời gian ủ, nhiệt độ ủ. Sự ảnh hưởng của nồng chiết điểm mù Mn(II) độ chất tạo phức PAN đến hiệu suất chiết đã Các yếu tố ảnh hưởng đến hiệu suất CPE như: được nghiên cứu trong khoảng 5.10-6 - 6.10-5 M. pH, nồng độ PAN, nồng độ TX-100, nồng độ Hình 2 cho thấy hiệu suất chiết phụ thuộc vào NaCl (lực ion), nhiệt độ ủ, thời gian ủ đã được 179 nồng độ 8-HQ. Hiệu suất chiết cao nhất tại mẫu bị sôi, do đó cũng ảnh hưởng đến quá nồng độ PAN 5.10-5 M. trình tách pha. Sự phụ thuộc của hiệu suất chiết vào nhiệt độ đã được khảo sát trong khoảng nhiệt độ từ 70oC đến 95oC. Tại nhiệt độ 90oC hiệu suất chiết đạt cao nhất. Thời gian chiết đã được nghiên cứu trong khoảng từ 10 - 80 phút. Tại thời gian 50 phút, hiệu suất chiết cao nhất đạt 91,2%. Lực ion ảnh hưởng đến quá trình tạo mixen keo. Trong nghiên cứu này, dùng NaCl để điều chỉnh lực ion. Khoảng nồng độ NaCl từ 0 – 0,5% đã được khảo sát. Giá trị nồng độ NaCl tối ưu là 0,5%. Hình 2. Ảnh hưởng của nồng độ 8-HQ đến 3.2. Khảo sát sự xen lấn của các cation khác hiệu suất CPE Mn(II) Một số cation có khả năng tạo phức với PAN [Mn(II)]: 0,2 ppm, pH 10, [TX-100]: 0,4%(v/v) và bị chiết vào pha chất hoạt động bề mặt, do 3.1.3. Sự ảnh hưởng của nồng độ TX-100 đó có thể gây ảnh hưởng đến quá trình chiết Hiệu suất chiết điểm mù phụ thuộc vào nồng của Mn(II). Sự phụ thuộc của hiệu suất chiết độ Triton X-100. Khi nồng độ chất hoạt động Mn(II) vào nồng độ của các cation Mg2+, Ca2+, bề mặt TX-100 thấp sẽ không hòa tan hết Zn2+, Ni2+, Cu2+, Pb2+, Co2+, Fe3+, Al3+, Cr3+ đã phức. Khi nồng độ TX-100 cao sẽ làm tăng độ được nghiên cứu. Kết quả cho thấy các cation nhớt, do đó làm giảm tín hiệu phân tích. Khảo không có kh ả năng tạo phức với PAN như sát với khoảng nồng độ TX-100 từ 0,05 % đến Mg2+, Ca2+ ở nồng độ lớn (1000 ppm) nhưng 0.8 %. Quá trình chiết đảm bảo định lượng ở ảnh hưởng không đáng kể đến hiệu suất chiết nồng độ TX-100 ≥ 0,2%, cao nhất tại 0,4%. Mn(II), những cation có khả năng tạo phức với Nên, nồng độ TX-100 0,4% được lựa chọn là PAN ở tỉ số nồng độ: [Mn+]/[Mn2+] = 50 ít xen nồng độ chất hoạt động bề mặt tối ưu. Kết quả lấn đến chiết điểm mù Mn(II). được chỉ ra ở hình 3. 3.3. Đặc điểm phân tích Dựng đường chuẩn CPE Mn(II) trong khoảng nồng độ 0.1- 5.0 ppm với điều kiện tối ưu. phương trình đường chuẩn: Abs = 0,0548.CMn + 0,0034 với hệ số tương quan R2 = 0,997. LOD và LOQ được xác định bằng cách tiến hành song song 18 dung dịch chứa 0,05 µg Mn(II) trong 10 mL. Dùng đường chuẩn đã xây dựng được để đo độ hấp thụ Mn, độ lệch chuẩn SD = 0.000513, tính được LOD và LOQ lần lượt là 0.0308 ppm và 0.0935 ppm. Hệ số Hình 3. Sự ảnh hưởng của nồng độ TX-100 đến làm giàu được tính bằng tỉ số giữa độ dốc của hiệu suất CPE Mn(II) đường chuẩn sử dụng chiết điểm mù và không -4 [Mn(II)]: 0,2 ppm, pH 10, [PAN]: 4.10 M sử dụng chiết điểm mù [0]. Phương trình 3.1.4. Sự ảnh hưởng của nhiệt độ chiết, thời đường chuẩn không sử dụng chiết điểm mù là gian chiết và lực ion Abs = 0,0066.CMn + 0,0011 với hệ số tương Nhiệt độ có ảnh hưởng lớn đến hiệu suất chiết quan R2 = 0,998. Hệ số làm giàu tính được là điểm mù. Khi nhiệt độ thấp, quá trình tạo 8,3. mixen keo và tách pha không thuận lợi. Khi 3.4. Phân tích mẫu chè nhiệt độ quá cao dẫn đến hiện tượng dung dịch 180 Sử dụng phương pháp vô cơ hóa ướt và FAAS hàm lượng Mn chiết tăng không đáng kể vì xác định hàm lượng Mn trong lá chè và nước hàm lượng Mn bị chiết đã đạt đến giá trị giới chè, kết quả được chỉ ra trong bảng 3. Mẫu chè hạn. thu hái tại bản Mống Vàng có hàm lượng Mn So sánh hàm lượng Mn trong lá chè và nước cao nhất là 877 mg/kg. Mẫu chè thu hái tại bản chè trong nghiên cứu này với một số nghiên Tà Xùa A có hàm lượng Mn thấp nhất là 513 cứu khác thu được kết quả được trình bày mg/kg. Hàm lượng Mn trong các mẫu chè thu trong bảng 4. hái tại 6 địa điểm của xã Tà Xùa chênh lệch nhau không quá nhiều có thể do thành phần hóa học trong đất trồng chè của các điểm này tương đương nhau. Phần trăm Mn chiết trong nước chè trong 5 phút, 15 phút và 30 phút lần lượt là 17,0 - 33,7%, 24,2 - 54,0% và 32,0 – 56,6%. Khi tăng thời gian chiết từ 5 phút lên 15 phút thì hàm lượng Mn chiết vào nước chè tăng lên. Khi tăng thời gian chiết từ 15 phút lên 30 phút thì Bảng 3. Hàm lượng Mn tổng trong lá chè, hàm lượng Mn trong nước chè theo thời gian Mn trong nước chè Tổng Mn Mẫu trong lá chè 5 phút 15 phút 30 phút (mg/kg) Mn chiết Tỷ lệ Mn chiết Tỷ lệ Mn chiết Tỷ lệ (mg/kg) chiết (%) (mg/kg) chiết (%) (mg/kg) chiết (%) CT1 801 136 17.0 360 44.9 347 43.3 CT2 602 184 30.6 325 54.0 341 56,6 TXA 513 173 33.7 244 47.6 238 46.4 TXC 625 155 24.8 192 30.7 185 29.6 BB 612 149 24.3 148 24.2 196 32.0 MV 877 168 19.2 339 38.7 345 39.3 Ghi chú: n = 3 lần thí nghiệm, độ tin cậy 95%. Bảng 4. Hàm lượng Mn trong mẫu chè của một số nghiên cứu Mn trong nước chè Mn trong lá chè Tham Mẫu chè (mg/kg) Hàm lượng Mn khảo Thời gian (mg/kg) 01 mẫu Vietnam Ché ngon So, Đun sôi 5 phút 197 Tam Đường, Lai Châu, Việt 943 Đun sôi 60 phút 423 17 Nam Đun sôi 24h 489 8 mẫu chè xanh Mộc Châu, Sơn 192 - 1169 Đun tới sôi 90,3 - 571 13 La, Việt Nam 10 mẫu chè xanh tỉnh Yên Bái, 478 - 2149 - - 18 Việt Nam 181 9 mẫu chè xanh tỉnh Tuyên 409 - 1127 - - 18 Quang, Việt Nam 10 mẫu chè xanh tỉnh Thái 694 – 1424 Đun tới sôi 179 - 413 14 Nguyên, Việt Nam Đun sôi 3 – 7 10 mẫu chè tiêu thụ tại Ba Lan 277 - 860 60 - 136 19 phút 6 mẫu chè xanh tại xã Tà Xùa, Nghiên Đun sôi 5, 15, 30 huyện Bắc Yên, tỉnh Sơn La, 513 - 877 136 - 360 cứu phút Việt Nam này Ứng dụng phương pháp CPE-FAAS xác định CPE - FAAS để xác định dạng Mn trong nước hàm lượng Mn tổng chiết, hàm lượng dạng chè đối với hai mẫu chè tại tỉnh Thái Nguyên. Mn(II)-flavonoid (dạng Mn liên kết hữu cơ) và Hàm lượng dạng Mn(II)-flavonoid trong nước dạng Mn(II) - tự do, phức yếu trong các mẫu chè chiếm gần 4,8%, hàm lượng dạng Mn(II) nước chè. Kết quả được trình bày trong bảng 5. tự do và phức yếu chiếm gần 95% [0]. S. Từ kết quả ở bảng 4 và bảng 5 nhận thấy hàm Yalçin và cộng sự ứng dụng phương pháp CPE lượng Mn tổng chiết trong nước chè xác định – FAAS phân tích một số mẫu chè tại Thổ Nhĩ bằng phương pháp vô cơ hóa ướt và phương Kỳ, dạng Mn(II)-flavonoid trong nước chè từ pháp CPE cho kết quả phù hợp nhau. Trong 10,3 µg/g đến 18,6 µg/g (chiếm 5%) còn dạng nước chè Tà Xùa, hàm lượng dạng Mn liên kết Mn(II) tự do và phức yếu từ 213 µg/g đến 364 với flavonoid chiếm 6,05 - 15,3%, còn lại dạng µg/g (chiếm 95%) [0]. Yüksel Ӧzdemir và Mn tự do và phức yếu chiếm đa số. cộng sự đã phân tích dạng Mn trong nước chè Các tác giả Lê Sỹ Bình, Đào Văn Bảy và Vũ của một số mẫu chè Thổ Nhĩ Kỳ sử dụng Đức Lợi sử dụng phương pháp CPE xác định phương pháp đồng kết tủa, hàm lượng Mn tổng dạng Mn trong 8 mẫu chè huyện Mộc Châu, chiết trong nước chè trong khoảng 337 – 637 tỉnh Sơn La. Hàm lượng Mn(II) - flavonoid mg/kg chiếm 30% tổng Mn trong lá chè. Dạng trong nước chè chiếm 8 - 35%, dạng Mn - tự Mn liên kết hữu cơ trong hai mẫu chè lần lượt do và phức yếu chiếm 65 -92%. Nguyễn Thị bằng 14,7 ± 9.8 mg/kg (chiếm 3,49%) và 38,0 Hiên và cộng sự đã ứng dụng phương pháp ± 8,2 (chiếm 10,38%) [0]. Bảng 5. CPE-FAAS phân tích dạng Mn trong nước chè Mn – tự do, Thời gian Mn – flavonoid % Mn - Mẫu phức yếu CPE tổng Mn (phút) (mg/kg) flavonoid (mg/kg) 5 16.0 123 139 11.5 CT1 15 25.3 340 365 6.93 30 20.8 323 344 6.05 5 14.8 166 181 8.18 CT2 15 32.9 291 324 10.2 30 28.7 310 339 8,47 5 26.2 145 171 15.3 TXA 15 25.1 215 240 10.5 30 22.8 216 239 9.54 5 16.1 142 158 10.2 TXC 15 13.2 181 194 6.80 182 30 17.9 170 188 9.52 5 22.0 129 159 13.8 BB 15 16.1 131 147 11.0 30 25.1 166 191 13.1 5 23.0 143 166 13.9 MV 15 29.4 308 337 8.72 30 34.4 312 346 9.94 Ghi chú: n = 3 lần thí nghiệm, độ tin cậy 95%. 4. KẾT LUẬN 4. Lydia Ferrara, Domenico Montesano, Chiết điểm mù Mn(II) với thuốc thử PAN và Alfonso Senatore (2001), Il Farmaco, Vol. 56, chất hoạt động bề mặt Triton X-100 đã được p. 397- 401. nghiên cứu. Đã nghiên cứu tối ưu các điều kiện 5. H. Watanabe, H. Tanaka (1978), Talanta, chiết điểm mù Mn(II) như: pH, nồng độ PAN, Vol. 25, p.585–589. nồng độ TX-100, sự xen lấn của các ion khác, 6. H. Watanabe, T. Kamidate, S. Kawamorita, thời gian chiết, nhiệt độ chiết, lực ion. Hiệu K. Haraguchi, and M. Miyajima (1987), suất chiết cao nhất đạt 97,5%, đảm bảo theo Analytical Sciences, Vol. 3 (5), p. 433–436. yêu cầu của AOAC [0]. Đã xây dựng đường 7. T. Saitoh, Y. Kimura, T. Kamidate, H. chuẩn chiết điểm mù Mn(II) trong khoảng Watanabe, K. Haraguchi (1989), Analytical nồng độ từ 0.1 – 5.0 ppm với R2 = 0,997. Giới Sciences, Vol. 5 (5), p.577–581. hạn phát hiện (LOD) và giới hạn định lượng 8. H. Watanabe, T. Saitoh, T. Kamidate, K. (LOQ) lần lượt là 0.0398 mppm và 0.0935 Haraguchi (1992), Microchimica Acta, Vol. ppm và hệ số làm giàu của phương pháp là 8,3. 106 (1 - 2), p.83–90. Đã sử dụng phương pháp vô cơ hóa - FAAS 9. Alireza Rezaie Rod, Shahin Borhani, phân tích hàm lượng mangan trong lá chè và Farzaneh Shemirani (2006), European Food nước chè của 6 mẫu chè thu hái tại xã Tà Xùa, Research and Technology, Vol. 223: p. 649– huyện Bắc Yên, tỉnh Sơn La. Ứng dụng 653. phương pháp CPE – FAAS phân tích dạng 10. V.O. Doroschuk, S.O. Lelyushok, V.B. Mn(II) tổng chiết, dạng Mn(II)-flavonoid và Ishchenko, S.A. Kulichenko (2004), Talanta, dạng Mn(II) – tự do và phức yếu trong các mẫu Vol. 64 (4), p.853–856. nước chè. Trong nước chè, hàm lượng dạng 11. K. Pytlakowska, V. Kozik, M. Dabioch Mn(II)-flavonoid ứng với thời gian chiết 5 (2013), Talanta, Vol. 110, p.202–228. phút, 15 phút và 30 phút lần lượt là: 8,18 – 12. S. Yalçin, H. Filik, and R. Apak (2012), 15,3% , 6,80 – 11,0% và 6,05 - 13,1%, còn lại Journal of Analytical Chemistry, Vol. 67 (1), p. là dạng Mn(II) – tự do và phức yếu. 47–55. TÀI LIỆU THAM KHẢO 13. Lê Sỹ Bình, Vũ Đức Lợi, Đào Văn Bảy 1. Aleksander Yashin, Yakov Yashin and Boris (2019), Tạp chí phân tích Hóa, Lý và Sinh học, Nemzer (2013), American Journal of Tập 24 (2), tr. 31-37. Biomedical Sciences, Vol. 5(4), p. 226-241. 14. Nguyễn Thị Hiên, Lưu Thị Nguyệt Minh, 2. Zong-mao Chen, Zhi Lin (2015), Journal of Vũ Đức Lợi, Dương Tuấn Hưng, Lê Sỹ Bình Zhejiang University-Science B, Vol. 16(2), p. (2014), Tạp chí Hóa học, Tập 52 (6A), Tr. 88- 87-102. 92. 3. Justyna Brzezicha-Cirocka, Małgorzata 15. Viện Tiêu chuẩn Chất lượng Việt Nam Grembecka, Piotr Szefer (2016), (1986), TCVN 4320-1986 Environmental Monitoring and Assessment, 16. L. B. Conceição, and Sérgio L. C. Ferreira Vol. 188 : 183. (2006), Microchim Acta, Vol. 154, p.149–152. 183 17. Street R., Száková J., Drábek O., 20. Yüksel Ӧzdemir, Şefef Güçer (1998), Food Mládková L. (2006): Czech J. Food Sci, Chemistry, Vol. 61 (3), p. 313–317. Vol.24 (2), p. 62–71. 21. The Association of Official Analytical 18. Nguyen Thi Thao, Tran Thi Mai (2017), Chemists (2016), AOAC Official Methods of Vietnam Journal of Science and Technology, Analysis: Guidelines for Standard Method Vol. 55 (5A), p. 143-150. Performance Requirements. 19. L. Polechoska, M. Dambiec, A. Klink, A. Rudecki (2015), Journal of food and drug analysis, Vol. 23 (3), p. 486 -492. ____________________________________________________________________________ CHẾ TẠO THAN HOẠT TÍNH TỪ VỎ CÂY CHÙM NGÂY.... (Tiếp theo tr.176) TÀI LIỆU THAM KHẢO (horseradish tree biomass)”, Process 1. T. Sumathi and G. Alagumuthu “Kinetics Biochemistry, 2007, vol 42, pp 547-553. and thermodynamics of methylene blue 5. Olugbenga Solomon Bello, Bukola Adsorption Studies for Arsenic Removal Using Morenike Lasisi, Olamide Joshua Adigun & Activated Moringa oleifera”, Hindawi Vunain Ephraim. “Scavenging Rhodamine B Publishing Corporation International Journal dye using moringa oleifera seed pod”. of Chemical Engineering, 2014, Article ID Chemical Speciation & Bioavailability, 2017, 430417, Vol 29, No1, pp 120-134. 6pages 6. MubeenaAkhtar, S.Moosa, Hasany, 2. Wombo, Itodo A, Wuana and Charles O M.I.Bhanger, ShahidIqbal, “Sorption potential Oseghale1, “Adsorptive Potential of Acid of Moringa oleifera pods for the removal of Modified Moringa Oleifera Wastes for organic pollutants from aqueous solution”, Tannery Effluent Decontamination”, Journal Journal of Hazardous Materials, 2007, of Chemistry: Education Research and Volume 141, No 3, 22, pp 546-556. Practice, 2018, Volume 2, Issue 1, pp 1 - 8. 7. Nor Salmi Abdullah1, Mohd Hazwan 3. Olugbenga Solomon Bello1, Kayode Hussin, Syazrin Syima Sharifuddin and Adesina Adegoke1, Opeyemi Omowumi Muhammad Azroie Mohamed Yusof Akinyunni, “Preparation and characterization “Preparation and characterization of activated of a novel adsorbent from Moringa oleifera carbon from Moringa Oleifera Seed pod ”, leaf”, Appl Water Sci, 2015, DOI Sci.Int.(Lahore), 2017, 29(1), pp7-11. 10.1007/s13201-015-0345-4. 4. Haq Nawaz Bhatti, Beenish Mumtaz, Muhammad Asif Hanif, Raziya Nadeem “Removal of Zn(II) ions from aqueous solution using Moringa oleifera Lam. 184
File đính kèm:
 ung_dung_chiet_diem_mu_su_dung_1_2_pyridylazo_2_naphthol_va.pdf
ung_dung_chiet_diem_mu_su_dung_1_2_pyridylazo_2_naphthol_va.pdf

