Tuyển chọn vi khuẩn nội sinh rễ cây mía đường có khả năng hòa tan lân
Hiệu quả sử dụng lân thấp hơn 15% ở vụ đầu tiên nên lượng lân còn lại được lưu tồn trong đất dưới dạng cây trồng không hấp thu được, sử dụng vi khuẩn để hòa tan lượng lân khó tan trong đất là một trong những biện pháp triển vọng trong trồng mía đường bền vững. Mục tiêu của nghiên cứu là chọn được những dòng vi khuẩn nội sinh rễ mía đường hòa tan các dạng lân khó tan trong đất phèn. 23 dòng vi khuẩn phân lập từ mẫu rễ mía đường trồng trên đất phèn được sử dụng để tuyển chọn các vi khuẩn có khả năng hòa tan các dạng lân khó tan. Kết quả cho thấy có 20 dòng vi khuẩn bị giới hạn sinh trưởng lớn hơn 50% ở điều kiện có nồng độ độc chất Al3+ 100 mg/L trong khi giá trị này nhỏ hơn 50% ở điều kiện có nồng độ độc chất Fe2+ 200 mg/L. Ngoài ra, đã tuyển chọn được một số dòng vi khuẩn triển vọng hòa tan lân nhôm (HA1f, PB2e, PB3e), lân sắt (HA1f, PB2e) và lân can xi (HA1b, HA1f), với hàm lượng lân lần lượt là 11,5-13,3, 60,8-62,1 và 73,9-86,4 mg/L. Cần sử dụng hỗn hợp các dòng vi khuẩn đã tuyển chọn để kết hợp chức năng hòa tan các thành phần lân khó tan để cung cấp lân và hỗ trợ sinh trưởng cây mía đường trong điều kiện đồng ruộng

Trang 1

Trang 2
Trang 3
Trang 4

Trang 5

Trang 6

Trang 7
Tóm tắt nội dung tài liệu: Tuyển chọn vi khuẩn nội sinh rễ cây mía đường có khả năng hòa tan lân

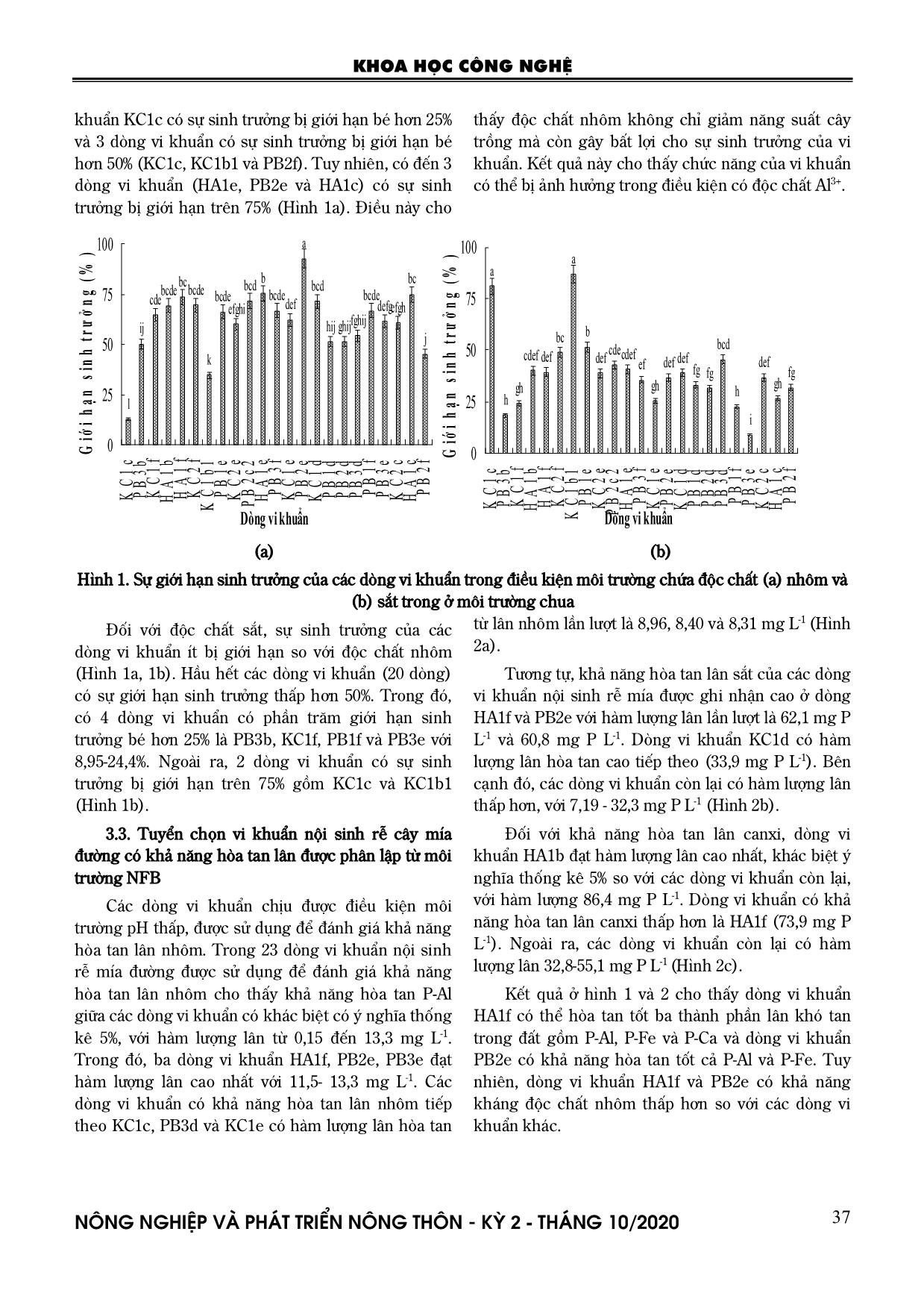
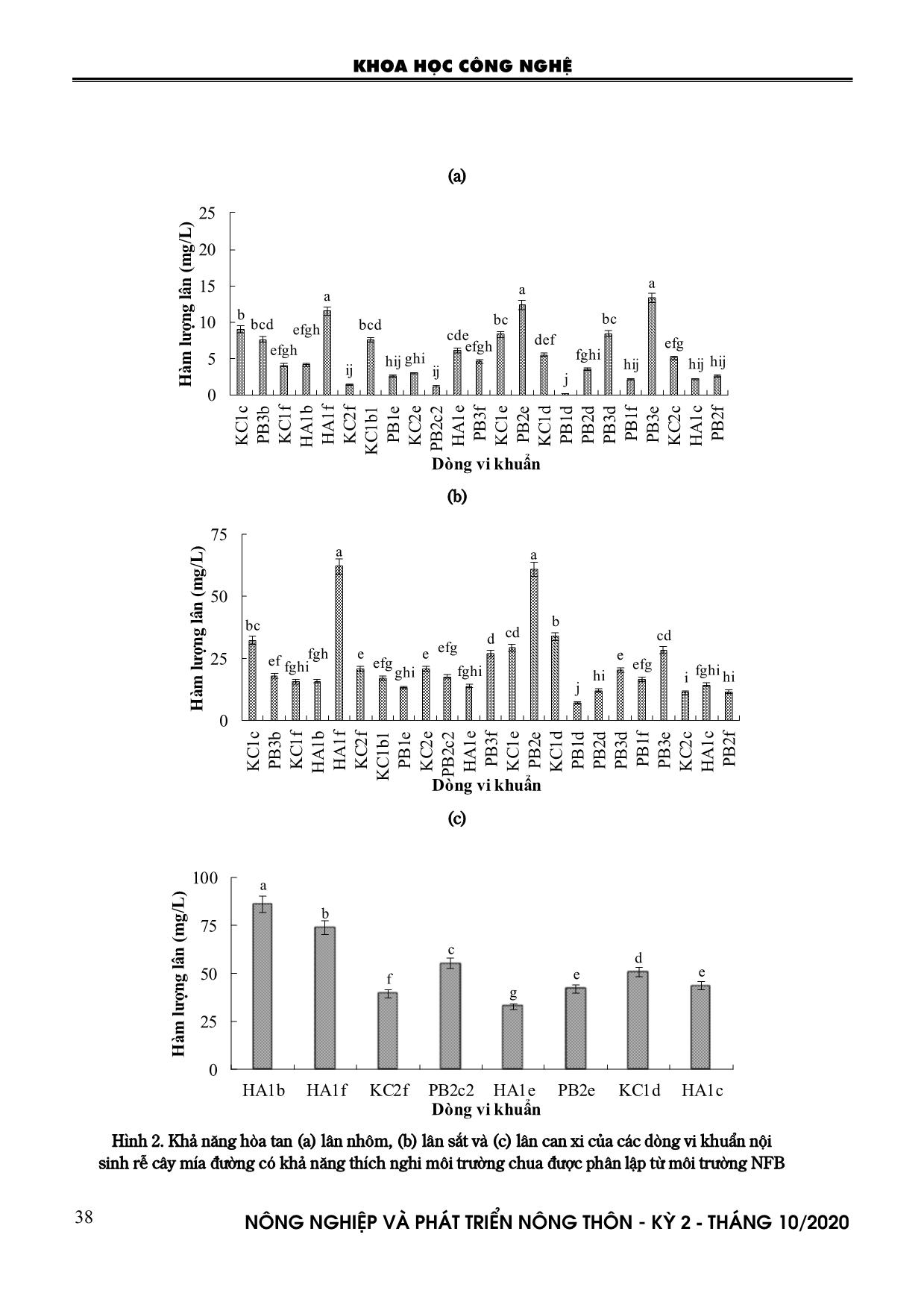
nhôm và (b) sắt trong ở môi trường chua Đối với độc chất sắt, sự sinh trưởng của các dòng vi khuẩn ít bị giới hạn so với độc chất nhôm (Hình 1a, 1b). Hầu hết các dòng vi khuẩn (20 dòng) có sự giới hạn sinh trưởng thấp hơn 50%. Trong đó, có 4 dòng vi khuẩn có phần trăm giới hạn sinh trưởng bé hơn 25% là PB3b, KC1f, PB1f và PB3e với 8,95-24,4%. Ngoài ra, 2 dòng vi khuẩn có sự sinh trưởng bị giới hạn trên 75% gồm KC1c và KC1b1 (Hình 1b). 3.3. Tuyển chọn vi khuẩn nội sinh rễ cây mía đường có khả năng hòa tan lân được phân lập từ môi trường NFB Các dòng vi khuẩn chịu được điều kiện môi trường pH thấp, được sử dụng để đánh giá khả năng hòa tan lân nhôm. Trong 23 dòng vi khuẩn nội sinh rễ mía đường được sử dụng để đánh giá khả năng hòa tan lân nhôm cho thấy khả năng hòa tan P-Al giữa các dòng vi khuẩn có khác biệt có ý nghĩa thống kê 5%, với hàm lượng lân từ 0,15 đến 13,3 mg L-1. Trong đó, ba dòng vi khuẩn HA1f, PB2e, PB3e đạt hàm lượng lân cao nhất với 11,5- 13,3 mg L-1. Các dòng vi khuẩn có khả năng hòa tan lân nhôm tiếp theo KC1c, PB3d và KC1e có hàm lượng lân hòa tan từ lân nhôm lần lượt là 8,96, 8,40 và 8,31 mg L-1 (Hình 2a). Tương tự, khả năng hòa tan lân sắt của các dòng vi khuẩn nội sinh rễ mía được ghi nhận cao ở dòng HA1f và PB2e với hàm lượng lân lần lượt là 62,1 mg P L-1 và 60,8 mg P L-1. Dòng vi khuẩn KC1d có hàm lượng lân hòa tan cao tiếp theo (33,9 mg P L-1). Bên cạnh đó, các dòng vi khuẩn còn lại có hàm lượng lân thấp hơn, với 7,19 - 32,3 mg P L-1 (Hình 2b). Đối với khả năng hòa tan lân canxi, dòng vi khuẩn HA1b đạt hàm lượng lân cao nhất, khác biệt ý nghĩa thống kê 5% so với các dòng vi khuẩn còn lại, với hàm lượng 86,4 mg P L-1. Dòng vi khuẩn có khả năng hòa tan lân canxi thấp hơn là HA1f (73,9 mg P L-1). Ngoài ra, các dòng vi khuẩn còn lại có hàm lượng lân 32,8-55,1 mg P L-1 (Hình 2c). Kết quả ở hình 1 và 2 cho thấy dòng vi khuẩn HA1f có thể hòa tan tốt ba thành phần lân khó tan trong đất gồm P-Al, P-Fe và P-Ca và dòng vi khuẩn PB2e có khả năng hòa tan tốt cả P-Al và P-Fe. Tuy nhiên, dòng vi khuẩn HA1f và PB2e có khả năng kháng độc chất nhôm thấp hơn so với các dòng vi khuẩn khác. KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 2 - TH¸NG 10/2020 38 (a) b bcd efgh efgh a ij bcd hij ghi ij cde efgh bc a def j fghi bc hij a efg hij hij 0 5 10 15 20 25 K C 1 c P B 3b K C 1 f H A 1 b H A 1 f K C 2 f K C 1 b1 P B 1e K C 2 e P B 2c 2 H A 1 e P B 3f K C 1 e P B 2e K C 1 d P B 1d P B 2d P B 3d P B 1f P B 3e K C 2 c H A 1 c P B 2f H àm l ư ợ n g lâ n ( m g /L ) Dòng vi khuẩn (b) bc ef fghi fgh a e efg ghi e efg fghi d cd a b j hi e efg cd i fghi hi 0 25 50 75 K C 1 c P B 3b K C 1 f H A 1 b H A 1 f K C 2 f K C 1 b1 P B 1e K C 2 e P B 2c 2 H A 1 e P B 3f K C 1 e P B 2e K C 1 d P B 1d P B 2d P B 3d P B 1f P B 3e K C 2 c H A 1 c P B 2f H àm l ư ợ n g lâ n ( m g /L ) Dòng vi khuẩn (c) a b f c g e d e 0 25 50 75 100 HA1b HA1f KC2f PB2c2 HA1e PB2e KC1d HA1c H àm l ư ợ n g lâ n ( m g /L ) Dòng vi khuẩn Hình 2. Khả năng hòa tan (a) lân nhôm, (b) lân sắt và (c) lân can xi của các dòng vi khuẩn nội sinh rễ cây mía đường có khả năng thích nghi môi trường chua được phân lập từ môi trường NFB KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 2 - TH¸NG 10/2020 39 Nhiều dòng vi khuẩn trong nghiên cứu này được xác định có khả năng hòa tan các thành phần lân khác nhau. Theo Rodrigues et al. (2017), có 47% trên tổng số vi khuẩn được phân lập từ các bộ phận lá, thân, rễ và đất vùng rễ mía có khả năng hòa tan lân khó tan. Cụ thể là dòng vi khuẩn Bacillus sp. ISO4 được phân lập từ lá mía có khả năng hòa tan lân P-Ca (Manoel da Silva et al., 2015; de Oliveira Silva et al., 2014) trong khi các dòng vi khuẩn Pseudomnas fluorescens, Pseudomonas putida-IL27A4Al, P. putida- IL28T1Al, Klebsiella terrigun có khả năng hòa tan P- Fe và P-Al (Premono et al., 1996). Trong đó, một số dòng vi khuẩn Burkholderia spp. được phân lập từ rễ mía có khả năng hòa tan lân trên môi trường thạch với bán kính 1,11-6,00 cm (Luvizotto et al., 2010). Bên cạnh đó, hai dòng vi khuẩn Bacillus sp. SCRU2 và Pseudomonas sp. SDRB4 hòa tan được lượng lân 11- 12 µg/L ở môi trường lỏng trong 48 giờ (Kaur và Putatunda, 2018), dòng vi khuẩn T-K5, T-K6 có hàm lượng lân được hòa tan 0,56 - 0,74 mg/L (Atekan et al., 2014). Do các dòng vi khuẩn có khả năng hòa tan lân nên khi áp dụng góp phần cải thiện dinh dưỡng trong cây, trong đất và dẫn đến gia tăng năng suất. Áp dụng dòng vi khuẩn Bacillus subtilis kết hợp Pseudomonas fluorescens giúp tăng hàm lượng lân trong lá mía, vi khuẩn Azospirillum brasilense kết hợp P. fluorescens giúp tăng hàm lượng lân trong đất, A. brasilense kết hợp B. subtilis giúp cải thiện sinh khối khô, tăng tổng hấp thu lân và dẫn đến tăng 38% năng suất và giảm được 75% phân lân cho cây mía (Rosa et al., 2020). Điều này cho thấy tiềm năng của các dòng vi khuẩn đã được tuyển chọn trong việc duy trì độ phì nhiêu đất như dưỡng chất lân để nâng cao hiệu quả kinh tế cũng như giảm được những ảnh hưởng bất lợi liên quan trực tiếp đến việc cung cấp lân cho cây trồng. 4. KẾT LUẬN VÀ ĐỀ NGHỊ 4.1. Kết luận Các dòng vi khuẩn nội sinh rễ cây mía đường sử dụng trong nghiên cứu có khả năng chịu được môi trường có chứa độc chất sắt tốt hơn môi trường có chứa độc chất nhôm ở điều kiện chua (pH 4,5). Tuyển chọn được các dòng vi khuẩn tiềm năng nhất hòa tan lân nhôm gồm HA1f, PB2e, PB3e, với 11,5-13,3 mg/L, lân sắt gồm HA1f, PB2e, với 60,8- 62,1 mg/L và lân can xi gồm HA1b, HA1f, với 73,9- 86,4 mg/L từ 23 dòng vi khuẩn nội sinh rễ cây mía đường. 4.2. Đề nghị Cần sử dụng các dòng vi khuẩn đã tuyển chọn để nâng cao hiệu quả cung cấp lân của đất cho cây mía trồng trên đất phèn trong điều kiện đồng ruộng. TÀI LIỆU THAM KHẢO 1. Attanandana, T., Vacharotayan, S. (1986). Acid sulfate soils: their characteristics, genesis, amelioration and utilization. Southeast Asian Studies. 24(2): 155–180. 2. de Oliveira Silva, M., Freire, F. J., Kuklinsky- Sobral, J., de Oliveira, E. C.A., dos Santos Freire, M. B. G., de Oliveira Apolinandario, V. E. X. (2016). Bacteria associated with sugarcane in Northeastern Brazil. African Journal of Microbiology Research. 10(37): 1586-1594. 3. Kalayu, G. (2019). Phosphate solubilizing microorganisms: Promising approach as biofertilizers. International Journal of Agronomy. 2019: 4917256. 4. Kaur, R., Putatunda, C. (2018). In vitro phosphate solubilization by sugarcane (Saccharum officinarum) rhizosphere bacteria. International Journal of Current Microbiology and Applied Sciences. 7(6): 1557-1564. 5. Khuong, N. Q., Kantachote, D., Onthong, J., Sukhoom, A. (2017). The potential of acid-resistant purple nonsulfur bacteria isolated from acid sulfate soils for reducing toxicity of Al3+ and Fe2+ using biosorption for agricultural application. Biocatalysis and Agricultural Biotechnology. 12: 329-340. 6. Kiflu, A., Beyene, S., Jeff, S. (2017). Fractionation and availability of phosphorus in acid soils of Hagereselam, Southern Ethiopia under different rates of lime. Chemical and Biological Technologies in Agriculture. 4(1): 1-7. 7. Luvizotto, D. M., Marcon, J., Andreote, F. D., Dini-Andreote, F., Neves, A. A., Araújo, W. L., Pizzirani-Kleiner, A. A. (2010). Genetic diversity and plant-growth related features of Burkholderia spp. from sugarcane roots. World Journal of Microbiology and Biotechnology. 26(10): 1829-1836. 8. Manoel da Silva, J., Carvalho dos Santos, T. M., Santos de Albuquerque, L., Coentro Montaldo, Y., Ubaldo Lima de Oliveira, J., Mesquita da Silva, S. G., Silva Nascimento, M., da Rocha Oliveira Teixeira, KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 2 - TH¸NG 10/2020 40 R. (2015). Potential of the endophytic bacteria (Herbaspirillum spp. And Bacillus spp.) to promote sugarcane growth. Australian Journal of Crop Science. 9(8): 754-760. 9. Martínez, M., Martínez, A. (2007). Effects of phosphate-solubilizing bacteria during the rooting period of sugar cane (Saccharum officinarum), Venezuela 51–71 variety, on the grower’s oasis substrate. In First International Meeting on Microbial Phosphate Solubilization (pp. 317-323). Springer, Dordrecht. 10. Murphy, J., Riley, H. P. (1962). A modified single solution method for the determination of phosphate in natural waters. Analytica Chimica Acta. 27: 31-36. 11. Murumkar, D. R., Nalawade, S. V., Indi, D. V., Pawar, S. M. (2017). Response of sugarcane seed plot to microbial inoculation by Gluconacetobacter diazotrophicus and phosphate-solubilizing bacteria. Sugar Tech. 19(1): 26-32. 12. Nguyễn Quốc Khương, Lê Vĩnh Thúc, Lê Thị Mỹ Thu, Lưu Thị Yến Nhi, Võ Văn Ựng, Trần Chí Nhân, Lý Ngọc Thanh Xuân và Nguyễn Thị Thanh Xuân, 2020. Phân lập, tuyển chọn vi khuẩn nội sinh rễ cây mía đường có khả năng cố định đạm và tổng hợp Indole Acetic Acid. Tạp chí Nông nghiệp và PTNT. 13. Nguyễn Quốc Khương, Ngô Ngọc Hưng, Nguyễn Kim Quyên (2014). Sử dụng kỹ thuật lô khuyết trong đánh giá sinh trưởng và đáp ứng năng suất mía vụ gốc trên đất phù sa ở đồng bằng sông Cửu Long. Chuyên đề Hướng tới nền nông nghiệp công nghệ cao và xây dựng nông thôn mới. Tạp chí Nông nghiệp và PTNT. Tháng 12 năm 2014. Trang 77 – 84. 14. Nguyễn Quốc Khương, Ngô Ngọc Hưng (2013). Ảnh hưởng của bón đạm, lân, kali kết hợp bã bùn mía lên sinh trưởng, độ Brix và năng suất của cây mía đường trên đất phù sa ở đồng bằng sông Cửu Long. Tạp chí Khoa học –Trường Đại học Cần Thơ. Số 29b: 70-77. 15. Nguyễn Quốc Khương, Ngô Ngọc Hưng (2014). Sử dụng kỹ thuật lô khuyết trong đánh giá dinh dưỡng khoáng đạm, lân và kali của cây mía trên đất phù sa đồng bằng sông Cửu Long. Tạp chí Nông nghiệp và PTNT. Số 3+4: 56-66. 16. Nguyễn Quốc Khương, Ngô Ngọc Hưng (2015a). Ảnh hưởng của bón khuyết NPK và bã bùn mía lên hấp thu NPK của cây mía vụ gốc trên đất phù sa tại Long Mỹ – Hậu Giang. Tạp chí Khoa học - Trường Đại học Cần Thơ. Số 40: 99-108. 17. Nguyễn Quốc Khương, Ngô Ngọc Hưng (2015b). Đánh giá khả năng cung cấp dưỡng chất bản địa của đất cho cây mía trên đất phù sa ở đồng bằng sông Cửu Long. Tạp chí Khoa học - Trường Đại học Cần Thơ. Số 39: 61-74. 18. Nguyễn Quốc Khương, Nguyễn Kim Quyên, Ngô Ngọc Hưng (2015a). Ảnh hưởng của bón N, P, K và bã bùn mía đến sinh trưởng và dinh dưỡng khoáng của cây mía tơ và mía gốc trên đất phù sa ở Long Mỹ - Hậu Giang. Tạp chí Khoa học và Phát triển. Tập 13, số 6: 885-892 19. Nguyễn Quốc Khương, Võ Thị Kim Phương, Ngô Ngọc Hưng (2015b). Ảnh hưởng của bón bã bùn mía và nấm Trichoderma đến sinh trưởng, năng suất và hấp thu NPK của mía đường trên đất phù sa tại Long Mỹ – Hậu Giang. Tạp chí Nông nghiệp và PTNT. Số 1: 58-65. 20. Premono, M. E., Anas, I., Soepardi, G., Hadioetomo, R. S., Saono, S., Sisworo, W. H. (1996). Improvement of p uptake and growth of sugarcane by phosphate-solubilizing microorganisms. Agriculture: Agronomy. 50-54. 21. Roberts, T. L., Johnston, A. E. (2015). Phosphorus use efficiency and management in agriculture. Resources, Conservation and Recycling. 105: 275-281. 22. Rodrigues, A. A., Forzani, M. V., Soares, R. D. S., Sibov, S. T., Vieira, J. D. G. (2016). Isolation and selection of plant growth-promoting bacteria associated with sugarcane. Pesquisa Agropecuária Tropica. 46(2): 149-158. 23. Rosa, P. A. L., Mortinho, E. S., Jalal, A., Galindo, F. S., Buzetti, S., Fernandes, G. C., Neto, N. B., Pavinato, P. S., Teixeira Filho, M. C. M. (2020). Inoculation with growth-promoting bacteria associated with the reduction of phosphate fertilization in sugarcane. Frontiers in Environmental Science. 8:32. 24. Samaranayake, P., Peiris, B. D., Dssanayake, S. (2012). Effect of excessive ferrous (Fe2+) on growth and iron content in rice (Oryza sativa). International Journal of Agriculture and Biology. 14, 296–298. 25. Sampanpanish, P., Ruangkhum, S., Tongcumpou, C. (2008). Effect of phosphorus in KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 2 - TH¸NG 10/2020 41 commercial fertilizers on phytoavailability cadmium and zinc uptake by sugarcane. WIT Transactions on Ecology and the Environment. 109: 739-749. 26. Soltangheisi, A., Santos, V. R. D., Franco, H. C. J., Kolln, O., Vitti, A. C., Dias, C. T. D. S., Herrera, W. F. B., Rodrigues, M., Soares, T. D. M., Withers, P. J. A., Pavinato, P. S. (2019). Phosphate sources and filter cake amendment affecting sugarcane yield and soil phosphorus fractions. Revista Brasileira De Ciência do Solo. 43: e0180227. 27. Sundara, B., Natarajan, V., Hari, K. (2002). Influence of phosphorus solubilizing bacteria on the changes in soil available phosphorus and sugarcane and sugar yields. Field Crops Research. 77(1): 43-49. SELECTION OF PHOSPHORUS SOLUBILIZING BACTERIA FROM SUGARCANE ROOT IN ACID SULFATE SOIL Nguyen Quoc Khuong, Le Vinh Thuc, Le Thi My Thu, Luu Thi Yen Nhi, Vo Van Ung, Tran Chi Nhan, Ly Ngoc Thanh Xuan, Nguyen Thi Thanh Xuan Summary The phosphorus use efficacy is lower than 15% in the first crop of P application, so bacterial use is one of the most promising methods to solubilize insoluble phosphorus forms for sustainable cultivation of sugarcane. The objective of this research was to select the endophytic bacteria from sugarcane root possessing the ability of insoluble phosphorus solubilization. From twenty-three colonies isolated from root samples of sugarcane grown in acid sulfate soil were used to select the promising phosphorus solubilizing bacteria. The results showed that almost endophytic bacterial strains (20 strains) were inhibited the growth by at least 50% under medium containing Al3+ at 100 mg/L while that of lower 50% under broth including Fe2+ at 200 mg/L. The selected strains of phosphorus solubilizing bacteria were included strains HA1f, PB2e, PB3e for Al-P solubilization, HA1f, PB2e for P-Fe solubilization and HA1b, HA1f for Ca-P solubilization, with their concentrations 11.5-13.3, 60.8-62.1 and 73.9-86.4 mg/L, respectively. Four selected strains were recommended to use in mixed cultures to produce available phosphorus and support the growth and yield of sugarcane. Keywords: Acid sulfate soil, endophytic bacteria from root, phosphorus solubilizing bacteria, sugarcane. Người phản biện: PGS.TS. Phan Quốc Hưng Ngày nhận bài: 20/3/2020 Ngày thông qua phản biện: 21/4/2020 Ngày duyệt đăng: 28/4/2020
File đính kèm:
 tuyen_chon_vi_khuan_noi_sinh_re_cay_mia_duong_co_kha_nang_ho.pdf
tuyen_chon_vi_khuan_noi_sinh_re_cay_mia_duong_co_kha_nang_ho.pdf

