Các thông số công nghệ của quá trình dịch hóa và đường hóa pyrodextrin để sản xuất maltodextrin kháng tiêu hóa từ tinh bột gạo
Mục đích của nghiên cứu nhằm xác định các thông số công nghệ phù hợp cho quá trình dịch hóa và đường hóa pyrodextrin để sản xuất maltodextrin kháng tiêu hóa từ tinh bột gạo. Các thông số công nghệ của quá trình dịch hóa bằng thủy phân enzim đã xác định được, bao gồm: nồng độ cơ chất 33-40%, nồng độ enzim α- amylase 0,4% (v/w chất khô), pH 5,8, nhiệt độ 95 - 97oC, thời gian thủy phân 60 ph. Chế độ công nghệ của quá trình đường hóa là: sử dụng cơ chất nối tiếp từ công đoạn dịch hóa với nồng độ 33-40% chất khô, enzim amyloglucosidase nồng độ 0,2%, pH 4,5, nhiệt độ 60oC, thời gian thủy phân 300 phút. Các chỉ tiêu chất lượng của sản phẩm thủy phân sau dịch hóa – đường hóa: Đương lượng dextrose 54 - 57, nồng độ chất khô hòa tan 29-31%, hàm lượng thành phần kháng tiêu hóa (IDF) 64-67%, hàm lượng chất xơ thực phẩm (TDF) 61 - 64%, protein < 0,6%,="" lipid="">< 0,04%,="" độ="" màu="" 65="" -="" 70.="" một="" sơ="" đồ="" quy="" trình="" công="" nghệ="" thủy="" phân="" pyrodextrin="" đã="" được="" đề="" xuất="" và="" kiểm="" định="" ở="" quy="" mô="" pilot="" (8="" kg/mẻ).="" kết="" quả="" cho="" thấy="" quy="" mô="" pilot="" khi="" áp="" dụng="" các="" thông="" số="" công="" nghệ="" đã="" đề="" xuất="" có="" chất="" lượng="" ổn="" định="" giữa="" các="" lần="" thủy="" phân,="" đồng="" thời="" đạt="" 90="" -="" 95%="" chất="" lượng="" so="" với="" sản="" phẩm="" thủy="" phân="" ở="" quy="" mô="" nhỏ="" phòng="" thí="" nghiệm="" 0,4="">

Trang 1

Trang 2

Trang 3
Trang 4

Trang 5

Trang 6

Trang 7

Trang 8
Tóm tắt nội dung tài liệu: Các thông số công nghệ của quá trình dịch hóa và đường hóa pyrodextrin để sản xuất maltodextrin kháng tiêu hóa từ tinh bột gạo

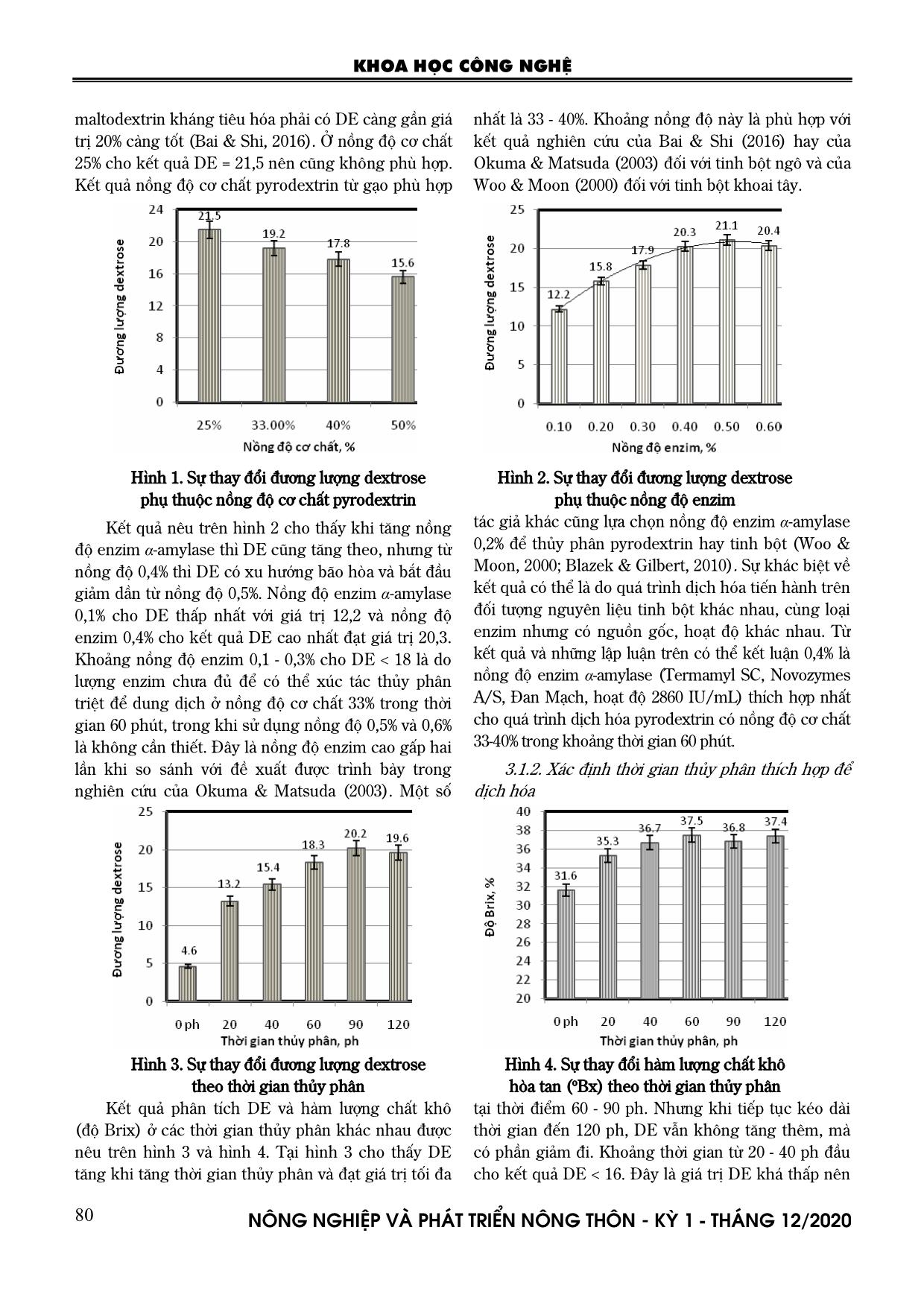
ương lượng dextrose phụ thuộc nồng độ cơ chất pyrodextrin Hình 2. Sự thay đổi đương lượng dextrose phụ thuộc nồng độ enzim Kết quả nêu trên hình 2 cho thấy khi tăng nồng độ enzim α-amylase thì DE cũng tăng theo, nhưng từ nồng độ 0,4% thì DE có xu hướng bão hòa và bắt đầu giảm dần từ nồng độ 0,5%. Nồng độ enzim α-amylase 0,1% cho DE thấp nhất với giá trị 12,2 và nồng độ enzim 0,4% cho kết quả DE cao nhất đạt giá trị 20,3. Khoảng nồng độ enzim 0,1 - 0,3% cho DE < 18 là do lượng enzim chưa đủ để có thể xúc tác thủy phân triệt để dung dịch ở nồng độ cơ chất 33% trong thời gian 60 phút, trong khi sử dụng nồng độ 0,5% và 0,6% là không cần thiết. Đây là nồng độ enzim cao gấp hai lần khi so sánh với đề xuất được trình bày trong nghiên cứu của Okuma & Matsuda (2003). Một số tác giả khác cũng lựa chọn nồng độ enzim α-amylase 0,2% để thủy phân pyrodextrin hay tinh bột (Woo & Moon, 2000; Blazek & Gilbert, 2010). Sự khác biệt về kết quả có thể là do quá trình dịch hóa tiến hành trên đối tượng nguyên liệu tinh bột khác nhau, cùng loại enzim nhưng có nguồn gốc, hoạt độ khác nhau. Từ kết quả và những lập luận trên có thể kết luận 0,4% là nồng độ enzim α-amylase (Termamyl SC, Novozymes A/S, Đan Mạch, hoạt độ 2860 IU/mL) thích hợp nhất cho quá trình dịch hóa pyrodextrin có nồng độ cơ chất 33-40% trong khoảng thời gian 60 phút. 3.1.2. Xác định thời gian thủy phân thích hợp để dịch hóa Hình 3. Sự thay đổi đương lượng dextrose theo thời gian thủy phân Hình 4. Sự thay đổi hàm lượng chất khô hòa tan (oBx) theo thời gian thủy phân Kết quả phân tích DE và hàm lượng chất khô (độ Brix) ở các thời gian thủy phân khác nhau được nêu trên hình 3 và hình 4. Tại hình 3 cho thấy DE tăng khi tăng thời gian thủy phân và đạt giá trị tối đa tại thời điểm 60 - 90 ph. Nhưng khi tiếp tục kéo dài thời gian đến 120 ph, DE vẫn không tăng thêm, mà có phần giảm đi. Khoảng thời gian từ 20 - 40 ph đầu cho kết quả DE < 16. Đây là giá trị DE khá thấp nên KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 1 - TH¸NG 12/2020 81 chưa đáp ứng yêu cầu của sản phẩm maltodextrin kháng tiêu hóa cần tạo ra. Bên cạnh đó, trong khoảng thời gian thủy phân 90 - 120 ph dù cho kết quả DE phù hợp nhưng cần thời gian thủy phân dài ở nhiệt độ cao có thể làm tăng biến màu dịch thủy phân. Từ hình 4 thấy rằng quá trình dịch hóa ở 0 - 40 ph đầu có độ Brix tăng nhanh, đạt mức cao nhất ở thời điểm 60 ph (37,5%), nhưng sau đó hầu như không thay đổi đáng kể. Kết hợp kết quả ở hình 3 và hình 4, thời gian thủy phân thích hợp nên chọn là 60 ph. Đây cũng là kết quả phù hợp với đề xuất của sáng chế US 0275253 A1 (Maeda et al., 2015). Tuy nhiên, kết quả thời gian này là ngắn hơn so với kết quả của Okuma & Matsuda (2003). 3.2. Nghiên cứu chế độ công nghệ thủy phân enzim để đường hóa pyrodextrin 3.2.1. Xác định nồng độ enzim và pH thích hợp để đường hóa pyrodextrin Hình 5. Sự thay đổi DE của sản phẩm đường hóa phụ thuộc nồng độ enzim AMG Hình 6. Sự thay đổi DE của sản phẩm đường hóa phụ thuộc pH thủy phân Bố trí 5 công thức với nồng độ enzim amyloglycosidase (AMG) 0,05%, 0,1%, 0,15%, 0,2%, 0,25% và 0,3% (tính theo chất khô pyrodextrin) để xác định nồng độ enzim cần thiết. Kết quả xác định DE nêu trên hình 5 cho thấy DE tăng dần theo chiều tăng của nồng độ enzim AMG, đạt giá trị cực đại ở nồng độ enzim 0,2% sau đó giảm dần ở các nồng độ 0,25 - 0,3%. Với nồng độ enzim AMG 0,2% cho kết quả DE là 57,4, giá trị này rất phù hợp với yêu cầu của sản phẩm kháng tiêu hóa mong đợi. Kết quả này là hoàn toàn phù hợp với một số công bố trước đây của nước ngoài (Okuma & Matsuda, 2003; Binder & McClain, 2010). Nhưng khi so sánh với kết quả nghiên cứu của Woo & Moon (2000) thì thấy các tác giả này chỉ dùng nồng độ enzim AMG 0,05% ở điều kiện pH và nồng độ cơ chất tương tự. Lý do có thể là do họ đã kéo dài thời gian thủy phân tới 48 giờ. Từ các nhận xét trên, có thể kết luận rằng nồng độ enzim AMG cần cho phản ứng đường hóa là 0,2%. Hình 6 trình bày sự phụ thuộc của trị số DE vào pH môi trường thủy phân. Từ hình thấy rằng DE có giá trị cao nhất trong khoảng pH 4,0 - 4,5 tương ứng với DE lần lượt là 54,9 và 57,7. Các điều kiện môi trường pH 5,0 - 6,0 là không phù hợp vì enzim bị ức chế làm giảm tốc độ phản ứng, nên DE giảm dần xuống chỉ còn 39,8. Binder & McClain (2010) cũng đề xuất pH 4,5 cho thủy phân đường hóa pyrodextrin. Như vậy, có thể khẳng định rằng pH 4,5 là thích hợp cho phản ứng đường hóa pyrodextrin để sản xuất maltodextrin kháng tiêu hóa từ tinh bột gạo. 3.2.2. Xác định nhiệt độ và thời gian thủy phân thích hợp để đường hóa pyrodextrin Hình 7 nêu kết quả xác định DE phụ thuộc vào nhiệt độ thủy phân ở 5 công thức nhiệt độ (50°C, 55°C, 60°C, 65°C, 70°C). Đánh giá số liệu kết quả thấy rằng khi nhiệt độ của phản ứng thủy phân tăng dần từ 50 - 70°C thì DE cũng tăng dần rồi đạt bão hòa ở 60°C, sau đó lại giảm dần. Ở nhiệt độ 60°C thu được DE cao nhất là 56,8. Quá trình đường hóa ở nhiệt độ cao hơn, từ 65 - 70°C nhưng kết quả DE thấp có thể do nhiệt độ cao làm ức chế enzim AMG. Tham chiếu với kết quả khác cho thấy sáng chế U.S. 9353392 B2 cũng đề xuất 60oC là nhiệt độ đường hóa tối ưu cho pyrodextrin (Maeda et al., 2015). Khảo sát ảnh hưởng của thời gian thủy phân tới chỉ số DE trong khoảng từ 120 - 360 ph có các số liệu kết quả nêu trên hình 8. Nhận thấy rằng đương lượng dextrose DE tăng dần theo thời gian và đạt cực KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 1 - TH¸NG 12/2020 82 đại DE = 57,9 ở 300 ph rồi bão hòa sau đó. Vì vậy, 300 ph hay 5 h được chọn là thời gian thích hợp để đường hóa pyrodextrin cùng với thời gian dịch hóa 1 h đã nêu ở mục 3.1.3. Thời gian đường hóa pyrodextrin theo các kết quả công bố của nước ngoài rất khác nhau, thường là dài hơn 5 h. Woo & Moon (2000) sử dụng nồng độ enzim AMG 0,05% nên chỉ đạt hiệu quả đường hóa sau 48 giờ. Maeda et al. (2015) giảm thời gian đường hóa còn 9 giờ khi đường hóa với nồng độ enzim 0,1%. Hầu hết các sáng chế ở Mỹ đều khuyến nghị đường hóa trong 24 giờ với nồng độ enzim 0,1% (Binder & McClain, 2010; Park et al., 2017). Sự khác biệt về thời gian đường hóa trong sản xuất maltodextrin kháng tiêu hóa có thể do nhiều lý do, chẳng hạn do khác nhau về cơ chất, nguồn gốc và hoạt độ enzim, yêu cầu về DE và hàm lượng thành phần kháng tiêu hóa của sản phẩm. Trong nghiên cứu này, kết quả thời gian đường hóa ngắn (5 giờ) là do sử dụng nồng độ enzim cao (0,2%) và có thể do các thông số thủy phân đã được tiệm cận tối ưu. Thời gian chỉ 5 giờ này rất có lợi cho thực tế sản xuất vì đã rút ngắn tới 1/5 - 1/2 so với thời gian của các công bố nước ngoài. Hình 7. Sự thay đổi DE của sản phẩm đường hóa phụ thuộc nhiệt độ thủy phân Hình 8. Sự thay đổi trị số DE của sản phẩm đường hóa phụ thuộc vào thời gian thủy phân 3.3. Quy trình công nghệ và kiểm định quy trình thủy phân pyrodextrin quy mô pilot Hình 9. Sơ đồ quy trình hòa trộn, dịch hóa, đường hóa pyrodextrin để sản xuất maltodextrin từ tinh bột gạo Từ các kết quả xác định thông số công nghệ thu được ở các mục nêu trên, một sơ đồ quy trình công nghệ hòa trộn - dịch hóa - đường hóa pyrodextrin được đề xuất nêu trên hình 9. Nguyên liệu là bột pyrodextrin cần đảm bảo chất lượng, đặc biệt là về hàm lượng thành phần kháng tiêu hóa IDF và độ trắng bột. Hàm lượng IDF > 65% và độ trắng > 60% được coi là chỉ tiêu chất lượng phải đạt của nguyên liệu bột pyrodextrin. Nếu độ trắng < 60% sẽ gặp nhiều khó khăn và tốn kém cho các công đoạn tinh chế. Quy trình có 5 công đoạn chính: 1- Hòa trộn bột pyrodextrin; 2- Dịch hóa; 3- Đường hóa; 4-Bất hoạt enzim và lọc loại tạp chất thô; 5- Kiểm tra chất lượng dịch thủy phân. Kiểm định quy trình được thực hiện 3 lần tương ứng với 3 mẻ thủy phân bằng thiết bị nấu dịch kiểu nồi lên men chịu áp lực. Nồi có thể tích 30 lít thích hợp cho thủy phân 8 kg bột pyrodextrin/mẻ, điều khiển tự động được nhiệt độ, tốc độ khuấy và thời gian. Kết quả xác định các thông số chất lượng của dịch thủy phân từ 3 mẻ được nêu trong bảng 1. Số liệu cho thấy sản phẩm có mức ổn định cao về chất lượng vì sự khác biệt giữa 3 mẻ sản xuất không đáng kể. Tuy nhiên, khi so sánh các thông số chất lượng giữa quy mô pilot và quy mô phòng thí nghiệm (0,4 kg/mẻ) thì xuất hiện sự khác nhau ở một số thông số như DE, IDF, TDF, độ Brix. Độ lệch về trị số của KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 1 - TH¸NG 12/2020 83 các chỉ tiêu này 5 - 10% là chấp nhận được khi thử nghiệm ở quy mô lớn. Nguyên nhân của sự chênh lệch các thông số sản phẩm giữa hai quy mô chưa được khảo sát, nhưng nhìn chung ở quy mô lớn thì tốc độ và thời gian cấp nhiệt hay làm mát là lớn hơn nhiều so với quy mô nhỏ. Tương tự, thời gian để điều chỉnh pH và bất hoạt cũng khác nhau. Bảng 1. Các thông số chất lượng của 3 mẻ sản phẩm dịch hóa - đường hóa Quy mô pilot 8 kg/mẻ Thông số đo Mẻ 1 Mẻ 2 Mẻ 3 Quy mô nhỏ phòng TN Đương lượng dextrose DE 54,6 53,9 56,3 57,9 Nồng độ chất khô hòa tan (%) 28,7 29,8 30,6 31,8 Thành phần kháng tiêu hóa IDF (%) 66,4 67,1 64,3 68,9 Chất xơ thực phẩm tổng số TDF (%) 61,7 63,5 60,8 65,3 Độ màu 69,3 66,7 65,2 58,8 Hàm lượng protein (%) 0,62 0,57 0,44 0,62 Hàm lượng chất béo (%) 0,05 0,03 0,04 0,07 4. KẾT LUẬN Đã xác định được các thông số của chế độ thủy phân để dịch hóa pyrodextrin: Nồng độ cơ chất pyrodextrin 33 - 40%, enzim α-amylase (Termamyl SC, hoạt độ 2860 IU/mL) nồng độ 0,4% tính theo khối lượng chất khô, pH 5,8 - 6,0, nhiệt độ 95 - 97oC, thời gian thủy phân 60 ph. Đã xác định được các thông số của chế độ thủy phân để đường hóa pyrodextrin: Công đoạn đường hóa nối tiếp công đoạn dịch hóa, cơ chất có nồng độ 33 - 40% ở công đoạn dịch hóa được sử dụng trực tiếp cho công đoạn đường hóa, enzym amyloglucosidase (Novozyme, hoạt độ 518 U/mL) nồng độ 0,2%, pH 4,0 - 4,5, nhiệt độ 60oC, thời gian đường hóa 300 phút. Đã kiểm định các thông số thủy phân để dịch hóa và đường hóa ở quy mô pilot 8 kg/mẻ, thu được kết quả ổn định về chất lượng sản phẩm trong các lần tiến hành thủy phân độc lập và đạt được 90 - 95% chất lượng so với kết quả ở quy mô thủy phân nhỏ phòng thí nghiệm. Từ đó đã đề xuất một quy trình công nghệ cho cụm công đoạn hòa trộn - dịch hóa - đường hóa pyrodextrin để sản xuất maltodextrin kháng tiêu hóa từ tinh bột gạo. TÀI LIỆU THAM KHẢO 1. Anderson J. W., Baird P., Davis R. H. Jr., Ferreri Knudtson M., Koraym A., et al. (2009). Health benefits of dietary fiber. Nutrition Reviews, 67, 188–205. 2. Association of Official Analytical Chemists – AOAC (2005). AOAC Official method 2001.03 Dietary fiber in foods containing resistant maltodextrin. In Official Methods of Analysis of the Association of Official Analytical Chemists. 14 ed. AOAC: Washington, DC. 3. Bai Y. & Shi Y. C. (2016). Chemical structures in pyrodextrin determined by nuclearmagnetic resonance spectroscopy. Carbohydrate Polymers, 151, 426–433. 4. Binder T., McClain J. (2010). Method of producing resistant starch and products formed therefrom. US Patent No.: 7,744,944 B2. 5. Blazek J., Gilbert E. P. (2010). Effect of enzymatic hydrolysis on nativestarch granule structure. Biomacromolecules, 11, 3275-3289. 6. Englyst H. N. & Hudson G. J. (1996). The classification and measurement of dietarycarbohydrates. Food Chemistry, 57, 15–21. 7. Laurentin A., Cárdenas M., Ruales J., Pérez E., Tovar J. (2003). Preparation of indigestible pyrodextrins from different starch sources. J. Agric. Food Chem, 51, 5510–5515. 8. Maeda Y., Shimada K., Katta Y. (2015). Method for producing indigestible dextrin. US Patent No.: US 2015/0275253 A1. 9. Nunes F. M., Lopes E. S., Moreira A. S., Simões J., Coimbra M. A., Domingues R. M. (2016). Formation of type 4 resistant starch and maltodextrins from amylose andamylopectin upon dry heating: A model study. Carbohydrate Polymers, 141, 253-262. 10. Okuma K. & Matsuda I. (2003). Production of indigestible dextrin from pyrodextrin. J. Appl. Glyosci., 50(3), 389-394. 11. Park J. W, Park S. W, Chong Jin Park C. J. (2017). Method for preparing digestion-resistant Maltodextrin. U.S. Patent 2017/0335020 A1. KHOA HỌC CÔNG NGHỆ N«ng nghiÖp vµ ph¸t triÓn n«ng th«n - KỲ 1 - TH¸NG 12/2020 84 12. Woo D. H., Moon T. W. (2000). Methods for preparing indigestible dextrin with high indigestible faction. Korean J. Food Sci Technol, 32(3), 610-617. 13. Yangilar F. (2013). The application of dietary fibre in food industry: Structural features, effects on health and definition, obtaining and analysis of dietary fibre: A review. Journal of Food and Nutrition Research, 1(3), 13-23. 14. Zhang B. J., Li X. X., Liu J., Xie F. W., Chen L. (2013). Supramolecular structure of A- and B-type granules of wheat starch. Food Hydrocolloids, 31, 68- 73. TECHNOLOGICAL PARAMETERS OF THE LIQUEFACTION AND SACCHARIFICATION FOR PRODUCING RESISTANT MALTODEXTRIN FROM RICE STARCH Pham Thi Binh, Bui Kim Thuy, Nguyen Duy Lam Summary The aim of the study was to determine the appropriate technological parameters for the liquefaction and saccharification of pyrodextrin for the production of resistant maltodextrin from rice starch. The technological parameters of the enzymatic liquefaction have been determined, including: substrate concentration 33 - 40%, concentration of α-amylase 0.4% (v/w dry matter), pH 5.8, temperature 95 - 97oC, hydrolysis duration 60 minutes. The technological mode of the saccharification is: using the serial substrate from the liquefaction stage with the concentration of 33 - 40% of the dry matter, the enzyme amyloglucosidase at the concentration of 0.2%, the pH 4.5 and the temperature of 60oC, hydrolysis duration 300 minutes. The quality criteria of the hydrolysis product after liquefaction and saccharification are: Dextrose equivalent 54 - 57, concentration of soluble dry mater 29 - 31%, content of indigestible fraction (IDF) 64 - 67%, content of total dietary fiber (TDF) 61 - 64%, protein <0.6%, lipid < 0.04%, level of color 65 - 70. A flow chard of pyrodextrin hydrolysis technology was proposed and tested at a pilot scale (8 kg/batch). The results show that the pilot scale when applying the proposed technological parameters is of stable quality between different batches and also achieving 90 - 95% quality compared to the product hydrolyzed at small laboratory scale. Keywords: Liquefaction, pyrodextrin, resistant maltodextrin, rice starch, saccharification. Người phản biện: PGS.TS. Tôn Thất Minh Ngày nhận bài: 17/8/2020 Ngày thông qua phản biện: 18/9/2020 Ngày duyệt đăng: 25/9/2020
File đính kèm:
 cac_thong_so_cong_nghe_cua_qua_trinh_dich_hoa_va_duong_hoa_p.pdf
cac_thong_so_cong_nghe_cua_qua_trinh_dich_hoa_va_duong_hoa_p.pdf

